题目内容
在氨水中存在下列电离平衡:NH3?H2O?NH4++OH-,下列情况能引起电离平衡向正向移动的有( )
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压.
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压.
| A、①③⑤ | B、①④⑥ |
| C、③④⑤ | D、①②④ |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氨水中存在下列平衡:NH3+H2O?NH3?H2O?NH4++OH-,加水促进电离,且如果加入能和铵根离子或氢氧根离子反应的物质,平衡就向电离方向移动,如果加入的物质中含有铵根离子或氢氧根离子,平衡向逆反应方向移动,以此解答该题.
解答:
解:①加NH4Cl固体,溶液中铵根离子浓度增大,平衡向逆反应方向移动,故①错误;
②加NaOH溶液,溶液中氢氧根离子浓度增大,平衡向逆反应方向移动,故②错误;
③加HCl,氢离子和氢氧根离子反应,导致平衡向右移动,故③正确;
④加CH3COOH溶液,氢离子和氢氧根离子反应,导致平衡向右移动,故④正确;
⑤加水促进电离,故⑤正确;
⑥因电离在溶液中进行,加压对溶液浓度影响不大,则平衡不移动,故⑥错误.
故选C.
②加NaOH溶液,溶液中氢氧根离子浓度增大,平衡向逆反应方向移动,故②错误;
③加HCl,氢离子和氢氧根离子反应,导致平衡向右移动,故③正确;
④加CH3COOH溶液,氢离子和氢氧根离子反应,导致平衡向右移动,故④正确;
⑤加水促进电离,故⑤正确;
⑥因电离在溶液中进行,加压对溶液浓度影响不大,则平衡不移动,故⑥错误.
故选C.
点评:本题考查了弱电解质的电离,为高频考点,注意把握影响弱电解质电离的因素,难度中等,注意加水稀释氨水电离平衡的移动,注意相关基础知识的积累.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
合理使用药物有利身心健康.下列说法正确的是( )
| A、因碘酒使蛋白质变性,故常用于外用消毒 |
| B、麻黄碱可用于止咳平喘,就是因为它能起到消炎作用 |
| C、长期大量使用阿司匹林有不良反应,应立即停药并静脉注射Na2CO3溶液 |
| D、能用于治疗胃酸过多的抗酸药有盘尼西林 |
用于净化汽车尾气的反应:2NO(g)+2CO(g)?2CO2(g)+N2(g),已知297℃时,该反应速率极慢,平衡常数为1×1059.下列说法正确的是( )
| A、提高尾气净化效率的最好方法是升高温度 |
| B、装有尾气净化装置的汽车排出的气体中一定不含NO或CO |
| C、297℃时该反应正向进行的程度很大,故使用催化剂并无实际意义 |
| D、提高尾气净化效率的最佳途径是研制高效催化剂 |
化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础.下列有关化学实验基本知识的描述不正确的是( )
| A、丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B、过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C、汽油和水的混合物可用分液的方法分离 |
| D、检验某溶液中是否含有SO42-的方法是先向该溶液中加入BaCl2溶液,再加入稀HNO3 |
下列各微粒的电子式正确的是( )
A、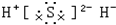 |
B、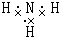 |
C、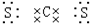 |
D、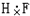 |
电子表中电源常用银-锌微型电池,电极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e-═ZnO+H2O;Ag2O+H2O+2e-═2Ag+2OH-电池的总反应式为:Ag2O+Zn═2Ag+ZnO,下列判断不正确的是( )
| A、锌为负极,Ag2O为正极 |
| B、锌发生还原反应,氧化银发生氧化反应 |
| C、原电池工作时,负极附近溶液的pH值减小 |
| D、原电池工作时,电子流动方向为Zn→Ag2O |
下列说法正确的是(NA为阿伏加德罗常数的值)( )
| A、标准状况下,2.24L的水的物质的量为0.1mol |
| B、标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
| C、10.0 g CaCO3和KHCO3的混合物中含有氧原子数为0.3NA |
| D、2.3 g Na与氧气完全反应,反应中转移的电子数介于0.1 NA到0.2NA之间 |