题目内容
2.常温下,测得0.1mol•L-1某溶液的pH值大于7,则该溶液中可能的溶质为( )| A. | KCl | B. | NH3 | C. | NaNO3 | D. | CH3COOH |
分析 常温下,0.1mol•L-1某溶液的pH值大于7,说明该溶液呈碱性,溶液中的溶质可能是碱性气体、碱或强碱弱酸盐,据此分析解答.
解答 解:常温下,0.1mol•L-1某溶液的pH值大于7,说明该溶液呈碱性,溶液中的溶质可能是碱、碱性气体或强碱弱酸盐,
A.KCl是强酸强碱盐,其水溶液呈中性,故A错误;
B.氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使其溶液呈碱性,故B正确;
C.硝酸钠是强酸强碱盐,其水溶液呈中性,故C错误;
D.醋酸是酸,在水溶液中电离出氢离子而导致溶液呈酸性,故D错误;
故选B.
点评 本题考查溶液酸碱性判断,为高频考点,侧重考查学生对元素化合物、弱电解质的电离、盐类水解的掌握和运用,注意:温度未知时不能根据溶液的pH判断溶液酸碱性,题目难度不大.

练习册系列答案
相关题目
13.五种短周期元素的某些性质如表所示,下列说法正确的是( )
| 元素代号 | X | W | Y | Z | Q |
| 原子半径(×10-12m) | 37 | 71 | 74 | 77 | 186 |
| 主要化合价 | +1 | -1 | -2 | +4、-4 | +1 |
| A. | X和Q都属于金属元素 | |
| B. | Y和Z的基态原子s能级和p能级电子数相同 | |
| C. | Y和W的第一电离能大小比较:Y>W | |
| D. | X、Z形成的化合物分子中可能既有σ键又有π键 |
10.常温常压下,下列物质为液态的是( )
| A. | 白银 | B. | 白磷 | C. | 乙烯 | D. | 水银 |
17.下列过程发生化学变化的是( )
| A. | 将水加热变成水蒸气 | |
| B. | 将蔗糖加入水中,得到蔗糖溶液 | |
| C. | 通过改变温度从空气中分离出氧气 | |
| D. | 向沸水中逐滴加入FeCl3饱和溶液,继续煮沸制备Fe(OH)3胶体 |
7.下列溶液中的溶质,不发生电离的是( )
| A. | 苏打水 | B. | 葡萄糖水 | C. | 稀盐酸 | D. | 生理盐水 |
14.氢气还原氧化铜:CuO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O,在该反应中( )
| A. | CuO作还原剂 | B. | 铜元素化合价降低 | ||
| C. | CuO作氧化剂 | D. | 铜元素化合价升高 |
5.碱式碳酸钴[Cox(OH)y(CO3)z]常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物.为了确定其组成,某化学兴趣小组同学设计了如图1所示的装置进行实验.
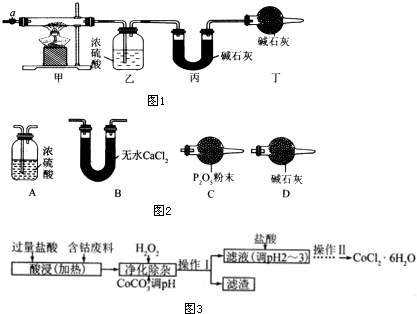
(1)请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中不再有气泡产生(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算.
(2)步骤④中缓缓通人空气数分钟的目的是将装置中生成的CO2和H2O全部排入乙、丙装置中.
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用图2装置中的D(填字母)连接在活塞a前(或装置甲前)(填装置连接位置).
(4)若按正确装置进行实验,测得如下数据.
则该碱式碳酸钴的化学式为Co3(OH)4(CO3)2.
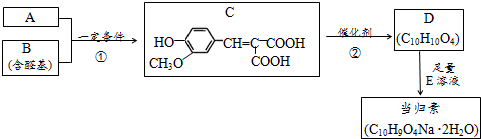
(5)CoCl2•6H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如图3:
已知:
①净化除杂时,加入 H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
②加入CoCO3 调pH为5.2~7.6,则操作1获得的滤渣成分为Fe(OH)3和Al(OH)3.
③加盐酸调整pH为2~3的目的为抑制CoCl2的水解.
④操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤.

(1)请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中不再有气泡产生(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算.
(2)步骤④中缓缓通人空气数分钟的目的是将装置中生成的CO2和H2O全部排入乙、丙装置中.
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用图2装置中的D(填字母)连接在活塞a前(或装置甲前)(填装置连接位置).
(4)若按正确装置进行实验,测得如下数据.
| 乙装置的质量/g | 丙装置的质量/g | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |
(5)CoCl2•6H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如图3:
已知:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
②加入CoCO3 调pH为5.2~7.6,则操作1获得的滤渣成分为Fe(OH)3和Al(OH)3.
③加盐酸调整pH为2~3的目的为抑制CoCl2的水解.
④操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤.
 ;
;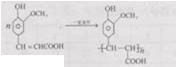 ;
;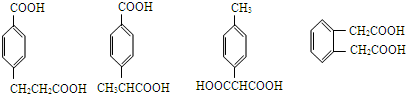 (其中两种).
(其中两种).
 .
.