题目内容
14.氢气还原氧化铜:CuO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O,在该反应中( )| A. | CuO作还原剂 | B. | 铜元素化合价降低 | ||
| C. | CuO作氧化剂 | D. | 铜元素化合价升高 |
分析 在氧化还原反应中失电子化合价升高的物质作还原剂,得电子化合价降低的物质作氧化剂,注意氧化剂、还原剂必须是反应物.
解答 解:A、该反应中氧化铜得电子化合价降低,所以氧化铜是氧化剂,故A错误;
B、该反应中氧化铜得电子化合价降低,铜元素化合价降低,故B正确;
C、反应前后,铜元素的化合价由+2价变为0价,CuO作氧化剂,故C正确;
D、反应前后,铜元素的化合价由+2价变为0价,所以铜元素的化合价降低,故D错误.
故选BC.
点评 本题考查了氧化还原反应,根据化合价变化来判断氧化剂、还原剂即可,注意氧化剂和还原剂都必须是反应物不是产物.

练习册系列答案
相关题目
4.下列实验操作正确的是( )


| A. | 用pH试纸测定浓硫酸的pH | |
| B. | 向碘酒中加入CCl4,静置后分液,可以分离碘酒中的碘 | |
| C. | 用甲图装置验证FeCl3对H2O2分解反应有催化作用 | |
| D. | 用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
2.常温下,测得0.1mol•L-1某溶液的pH值大于7,则该溶液中可能的溶质为( )
| A. | KCl | B. | NH3 | C. | NaNO3 | D. | CH3COOH |
9.出土的铜器文物表面有一层绿色的铜锈,铜锈的主要成分是( )
| A. | 碱式碳酸铜 | B. | 碳酸铜 | C. | 氢氧化铜 | D. | 氧化铜 |
19.下列气体能用向上排气法收集的有( )
| A. | NH3 | B. | H2 | C. | HCl | D. | CO2 |
6.经过长时间的努力已经可以解决部分的污染问题,例如可降解塑料的问世,聚二氧化碳塑料就是其中的佼佼者,有关聚二氧化碳塑料的说法正确的是( )
| A. | 聚二氧化碳塑料是通过缩聚反应生成的 | |
| B. | 聚二氧化碳塑料的结构式可表示为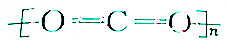 | |
| C. | 聚二氧化碳塑料属于纯净物,相对分子质量为44n | |
| D. | 聚二氧化碳塑料是属于环境友好材料 |
17.用NA表示阿伏德罗常数的数值,下列说法正确的是( )
| A. | 常温下,1mol•L-1的Na2CO3溶液中CO32-的数目小于NA | |
| B. | 常温常压下,1.7g NH3中所含的原子数为0.4NA | |
| C. | 向含0.1mol NH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目为0.4NA | |
| D. | 标准状况下,4.48LNO2与足量的水反应,转移的电子数为0.1NA |
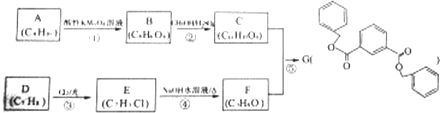
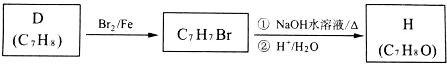
 .
.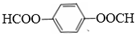 .
.