题目内容
15.质量相同的H216O和D216O所含质子数之比为10:9,中子数之比为8:9,分别与足量的金属钠反应生成气体在同温同压下体积之比为10:9.分析 根据n=$\frac{m}{M}$计算H216O和D216O的物质的量之比,H216O和D216O均含有10个质子,H216O和D216O含有中子数分别为8、10;
钠与水反应生成氢氧化钠与氢气,则生成氢气的物质的量之比等于H216O和D216O,同温同压下气体的体积之比等于其物质的量之比.
解答 解:根据n=$\frac{m}{M}$可知,等质量的H216O和D216O的物质的量之比为20g/mol:18g/mol=10:9,H216O和D216O均含有10个质子,则含有质子数之比为10:9,H216O和D216O含有中子数分别为8、10,则含有中子数之比为10×8:9×10=8:9;
钠与水反应生成氢氧化钠与氢气,则生成氢气的物质的量之比等于H216O和D216O,同温同压下气体的体积之比等于其物质的量之比,故二者生成氢气的体积之比为10:9,
故答案为:10:9;8:9;10:9.
点评 本题考查物质的量有关计算,比较基础,注意质子数、质子数、质量数之间关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是( )
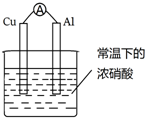

| A. | 电子由Al沿导线流向Cu | |
| B. | 电流由Cu电极流出 | |
| C. | Cu是原电池的负极 | |
| D. | 铝片上的电极反应式为:Al-3e-═Al3+ |
6.下列比较正确的是( )
| A. | 元素的电负性:S>P | B. | 晶体的硬度:碳化硅<晶体硅 | ||
| C. | 酸性:H3PO4<H3PO3 | D. | 热分解温度:CaCO3>BaCO3 |
3.下列有关电化学原理的说法中,错误的是( )
| A. | Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,铅为负极,PbO2为正极 | |
| B. | 电解氯化铜溶液,Cu2+向阴极迁移 | |
| C. | 氯碱工业中电解氯化钠溶液阴极产物为氯气 | |
| D. | 可充电的电池称“二次电池”,在充电时.是将电能转变成化学能,在放电时,又将化学能转化成电能 |
10.下列说法正确的是( )
| A. | 0.1mol•L-1的醋酸加水稀释,$\frac{c({H}^{+})}{c(O{H}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
20.对于可逆反应:2NO2(g)?N2O4(g)正反应放热.下列判断正确的是( )
| A. | 升高温度,混合气体颜色变浅 | |
| B. | 平衡时,NO2浓度必定等于N2O4浓度的两倍 | |
| C. | 平衡时,反应不在进行 | |
| D. | 平衡时,各组分浓度不再随时间的延长而发生变化 |
4.用萃取法从碘水中分离碘,所用萃取剂应具有的性质是( )
①不和碘或水起化学反应 ②能溶于水 ③不溶于水 ④应是极性溶剂 ⑤应是非极性溶剂.
①不和碘或水起化学反应 ②能溶于水 ③不溶于水 ④应是极性溶剂 ⑤应是非极性溶剂.
| A. | ①②⑤ | B. | ②③④ | C. | ①③⑤ | D. | ①③④ |