题目内容
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g) 4NO2(g)+O2(g)△H>0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确的是( )
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确的是( )
| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/(mol?L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
| A、500 s内N2O5分解速率为2.96×10-3mol?L-1?s-1 | ||
| B、T1温度下的平衡常数K1=125(mol?L-1)3,平衡时N2O5的转化率为50% | ||
| C、T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 | ||
D、达平衡后其他条件不变,将容器的体积压缩到原来的
|
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A.依据图标数据分析计算500s内N2O5(g)消耗的浓度计算分解率;
B.由表中数据可知,T1温度下,1000s时反应到达平衡,平衡时c(N2O5)=2.5mol/L,计算平衡浓度结合平衡常数概念计算平衡常数,计算转化率;
C.该反应正反应是吸热反应,升高温度,平衡向正反应移动,平衡常数增大;
D.将容器的体积压缩到原来的
,各物质的浓度先变为原来的2倍,而加压平衡左移.
B.由表中数据可知,T1温度下,1000s时反应到达平衡,平衡时c(N2O5)=2.5mol/L,计算平衡浓度结合平衡常数概念计算平衡常数,计算转化率;
C.该反应正反应是吸热反应,升高温度,平衡向正反应移动,平衡常数增大;
D.将容器的体积压缩到原来的
| 1 |
| 2 |
解答:
解答:解:A.依据图标数据分析计算500s内N2O5(g)消耗的浓度=5.00mol/L-3.52mol/L=1.48mol/L,分解速率=
=2.96×10-3 mol/(L?s),故A正确;
B.由表中数据可知,T1温度下,1000s时反应到达平衡,平衡时c(N2O5)=2.5mol/L,c(NO2)=5mol/L,c(O2)=1.25mol/L,平衡常数K=
=125,转化率为
×100%=50%,故B正确;
C.该反应正反应是吸热反应,升高温度,平衡向正反应移动,平衡常数增大,故C错误;
D.T1温度下,1000s时反应到达平衡,平衡时c(N2O5)=2.5mol/L,达平衡后其他条件不变,将容器的体积压缩到原来的
,各物质的浓度先变为原来的2倍,而加压平衡左移,则c(N2O5)>5.00 mol?L-1,故D正确;
故选C.
| 1.48mol/L |
| 500s |
B.由表中数据可知,T1温度下,1000s时反应到达平衡,平衡时c(N2O5)=2.5mol/L,c(NO2)=5mol/L,c(O2)=1.25mol/L,平衡常数K=
| [O2]?[NO2]4 |
| [N2O5]2 |
| 5-2.5 |
| 5 |
C.该反应正反应是吸热反应,升高温度,平衡向正反应移动,平衡常数增大,故C错误;
D.T1温度下,1000s时反应到达平衡,平衡时c(N2O5)=2.5mol/L,达平衡后其他条件不变,将容器的体积压缩到原来的
| 1 |
| 2 |
故选C.
点评:本题考查化学平衡状态判断、化学平衡有关计算、化学平衡影响因素、平衡常数等,难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
下列与有机物结构、性质相关的叙述错误的是( )
| A、用水可区分苯和溴苯 |
| B、蛋白质和油脂都属于高分子化合物,一定条件下都能水解 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 |
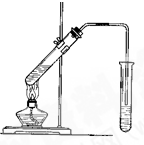 实验室用如图所示的装置制取乙酸乙酯.
实验室用如图所示的装置制取乙酸乙酯. 阅读下列材料后,回答相应问题.
阅读下列材料后,回答相应问题.