��Ŀ����
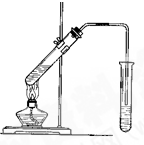 ʵ��������ͼ��ʾ��װ����ȡ����������
ʵ��������ͼ��ʾ��װ����ȡ������������1���ڴ��Թ�������һ���������Ҵ��������Ũ����Ļ��Һ�ķ����ǣ���
��2��װ����ͨ�����ĵ���Ҫ�嵽����̼������ҺҺ���ϣ������ܲ���Һ���У�ԭ���ǣ�
��3������̼������Һ��������
��4��ʵ����ȡ���������������ܶȱ�ˮ
��5����Ӧ�ķ���ʽ��
���㣺������������ȡ
ר�⣺
��������1����ȡ��������ʱ���ȼ���������Ҵ����ټ���Ũ���ᣬ��ֹ���Һ�彦��������Σ�գ�
��2�����ܲ��ܲ���Һ���µ�ԭ���Ƿ�ֹ������
��3������̼������Һ�����ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ����ڷֲ㣻�������Ҵ���Ũ���������¼��ȷ���������Ӧ���÷�ӦΪ���淴Ӧ��Ũ������ˮ����ƽ���������������������ƶ���
��4�����������������ϲ㣬�����ܶȱ�ˮС�����������������������ʷ�����
��5��������Ӧ�ı���Ϊ�����ǻ��������⣬�������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ���÷�ӦΪ���淴Ӧ��
��2�����ܲ��ܲ���Һ���µ�ԭ���Ƿ�ֹ������
��3������̼������Һ�����ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ����ڷֲ㣻�������Ҵ���Ũ���������¼��ȷ���������Ӧ���÷�ӦΪ���淴Ӧ��Ũ������ˮ����ƽ���������������������ƶ���
��4�����������������ϲ㣬�����ܶȱ�ˮС�����������������������ʷ�����
��5��������Ӧ�ı���Ϊ�����ǻ��������⣬�������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ���÷�ӦΪ���淴Ӧ��
���
�⣺��1����ȡ��������ʱ���ȼ���������Ҵ����ټ���Ũ���ᣬ��ֹ���Һ�彦��������Σ�գ��ʴ�Ϊ���ȼ���������Ҵ����ټ���Ũ���
��2���ӷ�������������Ҵ�������̼������Һ�����Ե��ܲ��ܲ���Һ���£�ԭ���Ƿ�ֹ�������ʴ�Ϊ����ֹ������
��3������̼������Һ���ջӷ����Ҵ��������ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ����ڷֲ㣻�������Ҵ���Ũ���������¼��ȷ���������Ӧ���÷�ӦΪ���淴Ӧ��Ũ������ˮ����ƽ���������������������ƶ���
�ʴ�Ϊ�����ջӷ����Ҵ��������ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ������á���ˮ���ã�
��4�����������������ϲ㣬�����ܶȱ�ˮС�������������з�����ζ���ʴ�Ϊ��С�����㣻
��5��������Ӧ�ı���Ϊ�����ǻ��������⣬�������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ���÷�ӦΪ���淴Ӧ��
�ʴ�Ϊ��CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O��
��2���ӷ�������������Ҵ�������̼������Һ�����Ե��ܲ��ܲ���Һ���£�ԭ���Ƿ�ֹ�������ʴ�Ϊ����ֹ������
��3������̼������Һ���ջӷ����Ҵ��������ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ����ڷֲ㣻�������Ҵ���Ũ���������¼��ȷ���������Ӧ���÷�ӦΪ���淴Ӧ��Ũ������ˮ����ƽ���������������������ƶ���
�ʴ�Ϊ�����ջӷ����Ҵ��������ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ������á���ˮ���ã�
��4�����������������ϲ㣬�����ܶȱ�ˮС�������������з�����ζ���ʴ�Ϊ��С�����㣻
��5��������Ӧ�ı���Ϊ�����ǻ��������⣬�������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ���÷�ӦΪ���淴Ӧ��
�ʴ�Ϊ��CH3COOH+CH3CH2OH
| Ũ���� |
| �� |
���������⿼�������������Ʊ������ʱ��ע��������Ӧ��ԭ���ͱ���̼������Һ�����ã���Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
���������ʰ��ᡢ��η������У���ȷ���ǣ�������
| A�����ᡢ���ʯ�� |
| B�����ᡢ�ռС�մ� |
| C�����ᡢ�Ҵ����Ȼ��� |
| D�����ᡢʳ�Ρ�ʯ��ʯ |
N2O5��һ����������������һ���¶��¿ɷ������·�Ӧ��2N2O5��g�� 4NO2��g��+O2��g����H��0
T1�¶�ʱ�����ܱ�������ͨ��N2O5������ʵ�����ݼ��±�������˵���в���ȷ���ǣ�������
T1�¶�ʱ�����ܱ�������ͨ��N2O5������ʵ�����ݼ��±�������˵���в���ȷ���ǣ�������
| t/s | 0 | 500 | 1000 | 1500 |
| c��N2O5��/��mol?L-1�� | 5.00 | 3.52 | 2.50 | 2.50 |
| A��500 s��N2O5�ֽ�����Ϊ2.96��10-3mol?L-1?s-1 | ||
| B��T1�¶��µ�ƽ�ⳣ��K1=125��mol?L-1��3��ƽ��ʱN2O5��ת����Ϊ50% | ||
| C��T1�¶��µ�ƽ�ⳣ��ΪK1��T2�¶��µ�ƽ�ⳣ��ΪK2����T1��T2����K1��K2 | ||
D����ƽ��������������䣬�����������ѹ����ԭ����
|
���и�����Һ�����������Լ����Ϳɽ����������ǣ�������
| A������ �������� ̼���� ����ͭ |
| B������ ������ �Ȼ��� ������ |
| C���������� ����þ �Ȼ��� ���� |
| D���Ȼ��� ������ �Ȼ��� ����� |
 �� X��Y��Z��W����Ԫ�أ�����X�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W��ԭ������Ϊ29���ش��������⣺
�� X��Y��Z��W����Ԫ�أ�����X�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W��ԭ������Ϊ29���ش��������⣺ ���淴ӦO2������+2SO2������?2SO3�������������ܱ������н��У�A��������һ���������ƶ��Ļ�����B �����ɱ��ֺ��� ����ͼ��ʾ������ش��������⣮
���淴ӦO2������+2SO2������?2SO3�������������ܱ������н��У�A��������һ���������ƶ��Ļ�����B �����ɱ��ֺ��� ����ͼ��ʾ������ش��������⣮
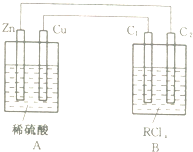 ij�������Ȼ���RClx13.5g����ˮ���0.100mol?L-1��ˮ��Һ1.00L��ȡ����Һ����ͼ��B�ձ��У����һ��ʱ�䣬Cu���Ϸų�11.2��������״�������壬B�ձ���C2������������0.0320g�������R�����ԭ��������
ij�������Ȼ���RClx13.5g����ˮ���0.100mol?L-1��ˮ��Һ1.00L��ȡ����Һ����ͼ��B�ձ��У����һ��ʱ�䣬Cu���Ϸų�11.2��������״�������壬B�ձ���C2������������0.0320g�������R�����ԭ��������