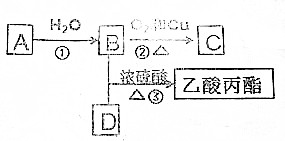
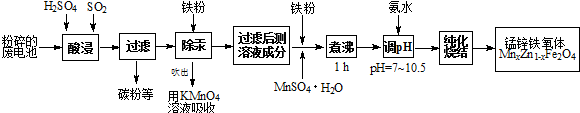
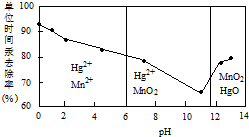
题目内容
5.W、X、Y、Z均是短周期元素,X、Y处于同一周期,电解含有X和Y的简单阴离子的混合溶液时,在阳极Y离子先失去电子.W和X同主族.Z的一种单质能在空气中自燃.对于这四种元素下列判断正确的是( )| A. | 单质的沸点:Z>X>Y | |
| B. | 单质的氧化性:W<Z<Y<X | |
| C. | 气态氢化物的稳定性:W>X>Y>Z | |
| D. | W单质可以将X从其盐溶液中置换出来 |
分析 W、X、Y、Z均是短周期元素,X、Y处于同一周期,电解含有X和Y的简单阴离子的混合溶液时,在阳极Y离子先失去电子,应为第三周期非金属元素,且非金属性X>Y,可知X为Cl、Y为S;W和X同主族,W为F.Z的一种单质能在空气中自燃,可知Z为P,然后结合元素周期律及元素化合物知识来解答.
解答 解:W、X、Y、Z均是短周期元素,X、Y处于同一周期,电解含有X和Y的简单阴离子的混合溶液时,在阳极Y离子先失去电子,应为第三周期非金属元素,且非金属性X>Y,可知X为Cl、Y为S;W和X同主族,W为F.Z的一种单质能在空气中自燃,可知Z为P,
A.P、S常温下为固体,S的沸点为444.6℃,P的沸点为280℃,单质的沸点:Y>Z>X,故A错误;
B.非金属性越强,单质的氧化性越强,则单质的氧化性:Z<Y<X<W,故B错误;
C.非金属性越强,氢化物越稳定,则气态氢化物的稳定性:W>X>Y>Z,故C正确;
D.W单质与水反应生成HF和氧气,则不能将X从其盐溶液中置换出来,故D错误;
故选C.
点评 本题考查位置、结构与性质的关系,为高频考点,把握X、Y为第三周期元素、离子的放电顺序推断元素为解答该题的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下表是 25℃时某些弱酸的电离平衡常数.
下列有关说法不正确的是( )
| 化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
| A. | 若H2C2O4 与等物质的量的 KOH反应后所得溶液呈酸性,则该溶液中各离子浓度由大到小的顺序为:c(K+)>c( HC2O4-)>c( H+)>c( C2O42-)>c( OH-) | |
| B. | 碳酸钠溶液中滴加少量氯水的离子方程式为:CO32-+Cl2+H2O=Cl-+HClO+HCO3- | |
| C. | 常温下,0.1mol/LCH3COOH 溶液加水稀释过程中,表达式c( H+)/c( CH3COOH )的数据变大 | |
| D. | pH相同的 NaClO 和 CH3COOK 溶液,其溶液的物质的量浓度的大小关系是:c( CH3COOK )>c( NaClO ) |
16. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)已知:2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-akJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-bkJ•mol-1
Cu(s)+$\frac{1}{2}$O2(g)=CuO(s)△H=-ckJ•mol-1
则方法I发生的反应:2Cu O(s)+C(s)=Cu2O(s)+CO(g);△H=2c-a-bkJ•mol-1.
(2)工业上很少用方法I制取Cu2O,是由于方法I反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因:若温度不当,会生成Cu.
(3)方法II为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.
该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;加热\;}}{\;}$2Cu2O+6H2O+N2.
(4)方法III采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,写出电极反应式
并说明该装置制备Cu2O的原理阴极电极反应:2H++2e-=H2↑,c(OH-)增大,通过阴离子交换膜进入阳极室,阳极电极反应:2 Cu-2e-+2OH-=Cu2O+H2O,获得Cu2O.
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0,水蒸气的浓度(mol/L)随时间t(min)
变化如下表所示.
下列叙述正确的是cd(填字母代号).
a.实验的温度:T2<T1
b.实验①前20min的平均反应速率v(O2)=7×10-5mol•L-1•min-1
c.实验②比实验①所用的Cu2O催化效率高
d. 实验①、②、③的化学平衡常数的关系:K1=K2<K3.
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:| 方法I | 用碳粉在高温条件下还原CuO |
| 方法II | 用肼(N2H4)还原新制Cu(OH)2 |
| 方法III | 电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-bkJ•mol-1
Cu(s)+$\frac{1}{2}$O2(g)=CuO(s)△H=-ckJ•mol-1
则方法I发生的反应:2Cu O(s)+C(s)=Cu2O(s)+CO(g);△H=2c-a-bkJ•mol-1.
(2)工业上很少用方法I制取Cu2O,是由于方法I反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因:若温度不当,会生成Cu.
(3)方法II为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.
该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;加热\;}}{\;}$2Cu2O+6H2O+N2.
(4)方法III采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,写出电极反应式
并说明该装置制备Cu2O的原理阴极电极反应:2H++2e-=H2↑,c(OH-)增大,通过阴离子交换膜进入阳极室,阳极电极反应:2 Cu-2e-+2OH-=Cu2O+H2O,获得Cu2O.
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0,水蒸气的浓度(mol/L)随时间t(min)
变化如下表所示.
| 序号 | Cu2O a克 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | 方法II | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | 方法III | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | 方法III | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
a.实验的温度:T2<T1
b.实验①前20min的平均反应速率v(O2)=7×10-5mol•L-1•min-1
c.实验②比实验①所用的Cu2O催化效率高
d. 实验①、②、③的化学平衡常数的关系:K1=K2<K3.
13.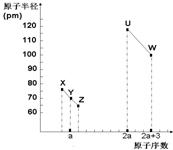 X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
 X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )
X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是( )| A. | U、X、W 三种元素最高价氧化物的水化物酸性依次增强 | |
| B. | 由Y、Z和氢三种元素形成的化合物中只有共价键 | |
| C. | XZ2、YZ2与X60的化学键类型和晶体类型都相同 | |
| D. | T元素与U同主族且在下一周期,能形成化合物TW4、TZ2、T3Y4 |
20.膜技术原理在化工生产中有着广泛的应用.有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下.下列说法不正确的是( )
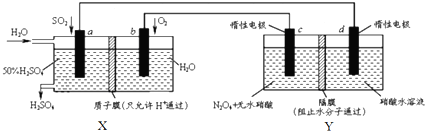

| A. | X是原电池,能够生产硫酸.Y是电解池,能够生产N2O5 | |
| B. | c电极的电极反应方程式为:N2O4+2HNO3-2e-=2N2O5+2H+ | |
| C. | 当电路中通过2mol e-,X、Y中各有1molH+从左边迁移到右边 | |
| D. | 为保证X中硫酸的质量分数不变,则加入的n(so2):n(H2O)=1:7.4 |
10.雾霾天气对环境影响很大.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
(1)室温下,吸收液吸收SO2的过程中,pH随n(SO32─):n(HSO3─)变化关系如下表:
①由表判断NaHSO3溶液显酸性,从原理的角度解释其原因在NaHSO3溶液中HSO3-存在HSO3-?H++SO32-和HSO3-+H2O?H2SO3+OH-两种平衡,HSO3-的电离程度大于其水解程度,故溶液呈酸性.
②在NaHSO3溶液中离子浓度关系不正确的是A(填序号).
A.c(Na+)=2c(SO32─)+c(HSO3─)
B.c(Na+)>c(HSO3─)>c(H+)>c(SO32─)>c(OH─)
C.c(H2SO3)+c(H+)=c(SO32─)+c(OH─)
D.c(Na+)+c(H+)=2c(SO32-)+c(HSO3─)+c(OH─)
③计算室温下HSO3─?H++SO32─的电离平衡常数K=6.3×10-8(保留2位有效数字).
(2)NaHSO3溶液在不同的温度下均可被过量的KIO3氧化,当NaHSO3完全消耗即有I2析出,将浓度均为0.02mol•L-1 的NaHSO3溶液(含少量淀粉)10.0mL和 KIO3(过量)酸性溶液40.0mL混合,记录溶液变蓝时间,实验结果如图.
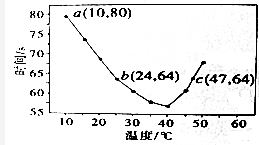
①由图可知,溶液变蓝的时间随温度的变化趋势是40℃之前,温度越高,溶液变蓝所需时间越短;40℃之后,温度越高,溶液变蓝所需时间越长.
40℃之后,淀粉不适宜用作该实验的指示剂(填“适宜”或“不适宜”),原因是:温度高于40℃时,碘与淀粉的显色反应灵敏度降低(或淀粉会糊化).
②b点和c点对应的反应速率的大小关系是ν (b)<ν (c)(填“>”、“<”或“﹦”).
(1)室温下,吸收液吸收SO2的过程中,pH随n(SO32─):n(HSO3─)变化关系如下表:
| n(SO32─):n(HSO3─) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
| c(H+)/mol•L─1 | 6.3×10─9 | 6.3×10─8 | 6.3×10─7 |
②在NaHSO3溶液中离子浓度关系不正确的是A(填序号).
A.c(Na+)=2c(SO32─)+c(HSO3─)
B.c(Na+)>c(HSO3─)>c(H+)>c(SO32─)>c(OH─)
C.c(H2SO3)+c(H+)=c(SO32─)+c(OH─)
D.c(Na+)+c(H+)=2c(SO32-)+c(HSO3─)+c(OH─)
③计算室温下HSO3─?H++SO32─的电离平衡常数K=6.3×10-8(保留2位有效数字).
(2)NaHSO3溶液在不同的温度下均可被过量的KIO3氧化,当NaHSO3完全消耗即有I2析出,将浓度均为0.02mol•L-1 的NaHSO3溶液(含少量淀粉)10.0mL和 KIO3(过量)酸性溶液40.0mL混合,记录溶液变蓝时间,实验结果如图.

①由图可知,溶液变蓝的时间随温度的变化趋势是40℃之前,温度越高,溶液变蓝所需时间越短;40℃之后,温度越高,溶液变蓝所需时间越长.
40℃之后,淀粉不适宜用作该实验的指示剂(填“适宜”或“不适宜”),原因是:温度高于40℃时,碘与淀粉的显色反应灵敏度降低(或淀粉会糊化).
②b点和c点对应的反应速率的大小关系是ν (b)<ν (c)(填“>”、“<”或“﹦”).
17.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为19.Y原子的电子层数与最外层电子数的比等于$\frac{1}{3}$,Z原子最外层电子数与内层电子数的比为$\frac{1}{10}$.下列说法正确的是( )
| A. | 非金属性:Y<X<W | |
| B. | 简单气态氢化物的热稳定性:Y<X | |
| C. | 化合物ZW、XY中化学键类型相同 | |
| D. | X、W的最高价氧化物的水化物均为强酸 |