题目内容
11.设NA 为阿伏加德罗常数的值.下列说法正确的是( )| A. | 标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA | |
| B. | 标准状况下,2.24L氯气中含有的Cl数目一定为0.2NA | |
| C. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 56 g的Fe与足量的稀盐酸完全反应转移电子数为3NA |
分析 A、标况下四氯化碳为液体;
B、求出氯气的物质的量,然后根据氯气为双原子分子来分析;
C、CO2与N2O的摩尔质量均为44g/mol,且均为三原子分子;
D、求出铁的物质的量,然后根据铁和稀盐酸反应后变为+2价来分析.
解答 解:A、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算物质的量,故A错误;
B、标况下2.24L氯气的物质的量为0.1mol,而氯气为双原子分子,故0.1mol氯气中含0.2NA个氯原子,故B正确;
C、CO2与N2O的摩尔质量均为44g/mol,故4.4g混合物的物质的量为0.1mol,且均为三原子分子,故0.1mol混合物中共含0.3NA个原子,故C正确;
D、56g铁的物质的量为1mol,而铁和稀盐酸反应后变为+2价,故1mol铁转移电子数为2NA个,故D错误.
故选BC.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 4mol浓盐酸与足量的二氧化锰反应生成1mol氯气 | |
| B. | 青铜是我国使用最早的合金,它的硬度和熔点都比铜的大 | |
| C. | 二氧化硅导电性能好,可用作光导纤维 | |
| D. | 液氨汽化时要吸收大量的热,可用作制冷剂 |
11.下列说法中,正确的是( )
| A. | SO2的摩尔质量是64 g | |
| B. | 标准状况下18 g水的体积是22.4 L | |
| C. | 14g N2含有的分子数为0.5NA | |
| D. | 1mol/LMgCl2溶液中含有Cl-的数目为2NA |
6.下列离子方程式正确的是( )
| A. | 硫酸铝溶液与过量Ba(OH)2溶液反应2Al3++3SO42-+3 Ba2++8OH-═3BaSO4↓+2A1O2-+4H2O | |
| B. | 碳酸钠溶液中滴加盐酸至恰好要出现气泡时停止:CO32-+2H+═CO2↑+H2O | |
| C. | 酸性高锰酸钾溶液与H2O2溶液混合:2MnO4-+3H2O2+6H+═2Mn2++6H2O+02↑ | |
| D. | 氯气通入亚硫酸钠溶液中:2Cl2+SO32-+H2O═2Cl-+SO2↑+2HClO |
16.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 298K 101kP时,22.4L CO2所含的原子数为3NA | |
| B. | 1mol Cl2与足量的Fe完全反应,转移的电子数为2NA | |
| C. | 0.5mol C2H2和C6H6的气态混合物中所含原子总数为2NA | |
| D. | 2L 1mol/L的盐酸中所含HCl分子数约为2NA |
3.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素.下列说法正确的是( )
| A. | 含D的盐溶液一定显酸性 | |
| B. | 可电解熔融DE3冶炼D单质 | |
| C. | 化合物AE与CE含有相同类型的化学键 | |
| D. | 1 mol 由元素A、B组成的化合物可能含有18 mol e- |
1.下列实验方法或操作正确的是( )
| A. | 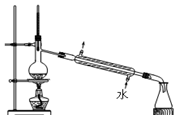 制蒸馏水 | B. | 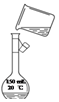 转移溶液 | ||
| C. | 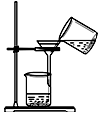 过滤 | D. | 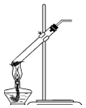 分解NaHCO3固体 |