题目内容
3.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素.下列说法正确的是( )| A. | 含D的盐溶液一定显酸性 | |
| B. | 可电解熔融DE3冶炼D单质 | |
| C. | 化合物AE与CE含有相同类型的化学键 | |
| D. | 1 mol 由元素A、B组成的化合物可能含有18 mol e- |
分析 A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,元素D是地壳中含量最多的金属元素,则D为Al元素,元素C在同周期的主族元素中原子半径最大,则C只能为Na元素;元素B的原子最外层电子数是其电子层数的2倍,B为第二周期的C元素,结合原子序及元素A、E的单质在常温下呈气态,E为Cl,A为H,以此来解答.
解答 解:由上述分析可知,A为H,B为C,C为Na,D为Al,E为Cl,
A.含D的溶液为偏铝酸盐时为碱性,为氯化铝时显酸性,故A错误;
B.氯化铝为共价化合物,熔融DE3不导电,故B错误;
C.HCl含共价键,NaCl含离子键,故C错误;
D.由元素A、B组成的化合物可为C2H6,质子数等于电子数,则1mol该化合物含有18 mol e-,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
2.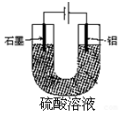 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )| A. | 阳极电极方程式为Al-3e+6OH-=Al2O3+3H2O | |
| B. | 随着电解的进行,溶液的pH逐渐增大 | |
| C. | 当阴极生成气体3.36L(标况)时,阳极增重2.4g | |
| D. | 电解过程中H+移向Al电极 |
3.下列物质的性质与应用的对应关系正确的是( )
| A. | MgO的熔点很高,可用于制造耐火材料 | |
| B. | (NH4)2SO4浓溶液能使蛋白质溶液发生盐析,可用于杀菌消毒 | |
| C. | 常温下Al与浓硝酸不反应,可以用铝槽车运输浓硝酸 | |
| D. | 碳具有强还原性,高温下能将二氧化硅还原为硅 |
11.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA | |
| B. | 标准状况下,2.24L氯气中含有的Cl数目一定为0.2NA | |
| C. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 56 g的Fe与足量的稀盐酸完全反应转移电子数为3NA |
18.下列实验操作与对应的实验目的或结论正确的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 往某溶液中加入BaCl2溶液产生白色沉淀 | 该溶液含有SO42- |
| B | 将氯气分别通入KI溶液和NaBr溶液中 | 证明还原性的强弱:I->Br->Cl- |
| C | 由Fe-Cu做电极,浓硝酸做电解质溶液组成的原电池 | 证明金属活泼性Fe>Cu |
| D | C2H5OH与浓硫酸170℃共热,制得的气体先通过足量的NaOH溶液,再通入酸性KMnO4溶液 | 使KMnO4溶液褪色的气体是乙烯 |
| A. | A | B. | B | C. | C | D. | D |
8.在含有0.4mol HNO3和0.2molHCl的混合酸1L中,加入0.3mol铜粉微热,充分反应后溶液中Cu2+的物质的量为( )
| A. | 0.15mol | B. | 0.225mol | C. | 0.3mol | D. | 无法计算 |
15.物质的用途体现性质.下列有关物质的用途和性质的说法中正确的是( )
| A. | 烧碱可以中和酸性土壤--烧碱显碱性 | |
| B. | 氮气可充入食品包装袋中防腐--氮气化学性质稳定 | |
| C. | 洗涤剂能清洗油污--洗涤剂能溶解油污 | |
| D. | 干冰可用于人工降雨--干冰升华放出热量 |