题目内容
15.除去NaCl溶液中混有的少量Na2SO4,以下加入的试剂和顺序合理的是( )| A. | BaCl2→Na2CO3→HCl | |
| B. | 过量的BaCl2→过量的Na2CO3→足量的HCl | |
| C. | 过量的Ba(NO3)2→过量的Na2CO3→HCl | |
| D. | Ba(OH)2→Na2CO3→HCl |
分析 除去NaCl溶液中混有的少量Na2SO4,选择氯化钡除去硫酸根离子,再利用碳酸钠除去过量的钡离子,最后加盐酸除去碳酸根离子,以此来解答.
解答 解:A.除杂试剂应过量,故A不选;
B.过量的BaCl2→过量的Na2CO3→足量的HCl可除去杂质,且不引入新杂质,故B选;
C.加过量的Ba(NO3)2引入新杂质硝酸根离子不能除去,故C不选;
D.除杂试剂应过量,故D不选;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,注意除杂试剂应过量、且除杂不能引入新杂质,题目难度不大.

练习册系列答案
相关题目
5.硫代硫酸钠(Na2S2O3)与稀H2SO4溶液时发生如下反应:Na2S2O3+H2SO4=Na2 SO4+SO2+S↓+H2O 下列反应速率最大的是( )
| A. | 0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水5mL,反应温度10℃ | |
| B. | 0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度10℃ | |
| C. | 0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度30℃ | |
| D. | 0.2mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度30℃ |
6.白酒、食醋、蔗糖、淀粉均为家庭厨房常用的物质,利用这些物质能完成下列实验的是( )
①检验自来水中是否含氯离子②鉴别食盐和小苏打 ③蛋壳能否溶于酸 ④白酒中是否含水.
①检验自来水中是否含氯离子②鉴别食盐和小苏打 ③蛋壳能否溶于酸 ④白酒中是否含水.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
3.已知某溶液中存在较多的SO42-、NO3-则溶液中还可能大量存在的离子组是( )
| A. | Fe3+、AlO2-、Cl- | B. | Na+、NH4+、S2- | C. | H+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |
10. 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
(2)同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(4)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,填写下列表达式中的数据变化情况(填“变大”、“变小”或“不变”)
①$\frac{{c(C{H_3}COOH)}}{{c({H^+})}}$变小;②$\frac{{c(C{H_3}CO{O^-})•c({H^+})}}{{c(C{H_3}COOH)}}$不变;
③$\frac{{c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)}}$变大;④$\frac{{c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)•c(O{H^-})}}$不变.
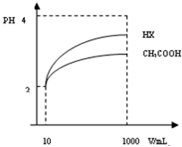
(5)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数:理由是当完全电离时应该是PH=4,现在PH值HX>CH3COOH,说明原来HX电离更多,故HX的电离平衡常数>醋酸的电离平衡常数.
 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
(2)同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(4)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,填写下列表达式中的数据变化情况(填“变大”、“变小”或“不变”)
①$\frac{{c(C{H_3}COOH)}}{{c({H^+})}}$变小;②$\frac{{c(C{H_3}CO{O^-})•c({H^+})}}{{c(C{H_3}COOH)}}$不变;
③$\frac{{c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)}}$变大;④$\frac{{c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)•c(O{H^-})}}$不变.
(5)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数:理由是当完全电离时应该是PH=4,现在PH值HX>CH3COOH,说明原来HX电离更多,故HX的电离平衡常数>醋酸的电离平衡常数.
20.下列仪器的使用、实验药品选择或实验现象描述正确的是( )
| A. | 苯、乙醇、四氯化碳都是重要有机溶剂,都可用于提取碘水中的碘单质 | |
| B. | 可用蘸浓硫酸的玻璃棒检验输送氨气的管道是否漏气 | |
| C. | 除去Fe(OH)3胶体中的NaCl时,可将其装在用半透膜做的袋子里,放在流动的蒸馏水中,该分离方法称为渗析 | |
| D. | 用量筒量取10.00mL 1.0mol/L的盐酸于100mL溶量瓶中,加水稀释至刻度,可制得0.1mol/L的盐酸 |
2.下列有机物中,一氯取代物有2种的是( )
①
②
③CH3CH2CH3
④
①

②

③CH3CH2CH3
④

| A. | 全部 | B. | ①③ | C. | ②④ | D. | ②③ |
 为测定硫酸钠晶体的化学式,取样品32.2g配成100mL溶液,再滴入5mol/L氯化钡溶液,当滴入20mL时恰好不再产生沉淀,试通过计算写出硫酸钠晶体的化学式.
为测定硫酸钠晶体的化学式,取样品32.2g配成100mL溶液,再滴入5mol/L氯化钡溶液,当滴入20mL时恰好不再产生沉淀,试通过计算写出硫酸钠晶体的化学式.
 H2O
H2O