题目内容
3.已知某溶液中存在较多的SO42-、NO3-则溶液中还可能大量存在的离子组是( )| A. | Fe3+、AlO2-、Cl- | B. | Na+、NH4+、S2- | C. | H+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |
分析 根据离子之间不能结合生成沉淀、气体、水、弱电解质等,不能发生氧化还原反应、相互促进水解等,则离子大量共存,以此来解答.
解答 解:A.Fe3+、AlO2-相互促进水解,不能大量共存,故A不选;
B.NH4+、S2-相互促进水解,不能大量共存,故B不选;
C.H+、NO3-、Fe2+发生氧化还原反应,不能大量共存,故C不选;
D.该组离子之间不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意水解反应、氧化还原反应的离子反应判断,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.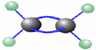 如图是某有机物分子的球棍式模型,其中大球代表碳原子,小球代表氢原子,短棍代表共价键,该有机物的名称是( )
如图是某有机物分子的球棍式模型,其中大球代表碳原子,小球代表氢原子,短棍代表共价键,该有机物的名称是( )
 如图是某有机物分子的球棍式模型,其中大球代表碳原子,小球代表氢原子,短棍代表共价键,该有机物的名称是( )
如图是某有机物分子的球棍式模型,其中大球代表碳原子,小球代表氢原子,短棍代表共价键,该有机物的名称是( )| A. | 乙烯 | B. | 乙烷 | C. | 乙醇 | D. | 乙炔 |
14.为除去H2S气体中混有的少量杂质HCl和CO2气体,应选用的试剂是( )
| A. | 饱和Na2S溶液 | B. | 饱和NaHCO3溶液 | C. | 饱和NaHS溶液 | D. | 饱和NaCl溶液 |
11.以下有关物质结构的描述正确的是( )
| A. | 甲苯分子中的所有原子可能共平面 | |
| B. | 苯乙烯分子中的所有原子一定共平面 | |
| C. | 二氯甲烷分子为正四面体结构 | |
| D. | 乙烷分子中的所有原子不可能共平面 |
8.下列有关实验的操作、原理和现象的叙述正确的是( )
| A. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 | |
| B. | 配制0.1 mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| C. | 用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 | |
| D. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用,迅速混合后测出初始温度,用环形玻璃搅拌棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 |
15.除去NaCl溶液中混有的少量Na2SO4,以下加入的试剂和顺序合理的是( )
| A. | BaCl2→Na2CO3→HCl | |
| B. | 过量的BaCl2→过量的Na2CO3→足量的HCl | |
| C. | 过量的Ba(NO3)2→过量的Na2CO3→HCl | |
| D. | Ba(OH)2→Na2CO3→HCl |
11.在密闭容器中进行如下反应:X2(气)+Y2(气)?2Z(气),已知 X2、Y2、Z的起始浓度分别为 0.1mol/L,0.3mol/L,0.2mol/L,在一定的条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | Z 为 0.3 mol/L | B. | Y2为 0.4 mol/L | C. | X2为 0.2 mol/L | D. | Z 为 0.4 mol/L |