题目内容
20.下列表达方式错误的是( )| A. | 甲烷的电子式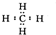 | B. | 碳-12原子:612C | ||
| C. | 氟化钠的电子式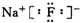 | D. | 硫离子的结构示意图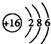 |
分析 A、甲烷为共价化合物,通过共用电子对形成化合物,电子式中不标电荷;
B、碳-12原子的核电荷数为6,质量数为12;
C、氟化钠为离子化合物,电子式中阴、阳离子的电荷应该标出;
D、硫原子得到两个电子形成硫离子,其核外电子为18.
解答 解:A、甲烷分子中含有四对碳氢共用电子对,其电子式为: ,故A正确;
,故A正确;
B、碳-12原子的质量数为12,核电荷数为6,可以表示为:612C,故B正确;
C、氟化钠的电子式中需要标出离子所带电荷,氟化钠的电子式为: ,故C正确;
,故C正确;
D、硫离子核外电子数为18,其结构示意图为: ,故D错误;
,故D错误;
故选D.
点评 本题考查常见化学用语的正误判断,题目难度中等,主要是考查学生对常见化学用语的熟悉掌握程度,需要学生熟练记住.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
5.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是( )
| A. | 用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 | |
| B. | 在组装蒸馏装置时,温度计的水银球应伸入液面下 | |
| C. | 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水 | |
| D. | 在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温才过滤 |
15.常温下,部分弱酸的电离平衡常数如表:
下列选项错误的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.8×10-5 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 等物质的量浓度时:pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa) | |
| B. | 中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者大于后者 | |
| C. | 向NaCN中通入少量的CO2:CN -+H2O+CO2=HCO3 -+HCN | |
| D. | 0.2mol/L HCN与0.1mol/L NaOH溶液等体积混合后显碱性,则c(Na+)>c(CN-) |
5.光导纤维的主要成分是SiO2,对于它的分类中正确的是( )
| A. | 酸性氧化物 | B. | 电解质 | C. | 离子化合物 | D. | 有机物 |
10.下列气体在同温同压时,密度最大的是( )
| A. | O2 | B. | SO2 | C. | Cl2 | D. | NH3 |
 .
.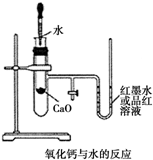 如图是某同学设计的放热反应的观察装置,其实验操作步骤如下:
如图是某同学设计的放热反应的观察装置,其实验操作步骤如下: