题目内容
13.下列各组物质中有极性共价键的是( )| A. | I2 | B. | MgCl2 | C. | KCl | D. | H2O |
分析 极性共价键是有不同非金属元素的原子形成的共价键,如水分子中含有极性键,而碘单质中含有的是非极性键,氯化镁和氯化钾中只含有离子键,据此进行判断.
解答 解:A.I2分子中只含有非极性共价键,故A错误;
B.MgCl2为离子化合物,MgCl2中只含有离子键,故B错误;
C.NaCl为离子化合物,NaCl中只含有离子键,故C错误;
D.H2O为共价化合物,其分子中的O-H键为极性共价键,故D正确;
故选D.
点评 本题考查了共价键类型及判断方法,题目难度不大,明确常见化学键类型为解答关键,注意明确极性共价键与非极性共价键的区别,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列说法错误的是( )
| A. | O3与SO2的结构相似 | B. | 硫粉不溶于水,易溶于CS2中 | ||
| C. | Be(OH)2是两性氢氧化物 | D. | 在相同条件下,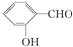 的沸点高于 的沸点高于 |
1.在测溶液的性质时,下列试纸中预先不能用蒸馏水润湿的是( )
| A. | 石蕊试纸 | B. | PH试纸 | C. | KI淀粉试纸 | D. | 醋酸铅试纸 |
8.已知短周期元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 氢化物的稳定性H2Y>HZ | B. | 离子半径W3+<Z-,第一电离能X<W | ||
| C. | W、X、Y、Z最高正价与族序数相等 | D. | 电负性Z<Y<W<X |
5.下列有关“化学与生活”的叙述不正确的是( )
| A. | 漂白粉漂白织物利用了物质氧化性 | |
| B. | 点燃爆竹后,硫燃烧生成SO2 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | PX项目的主要产品对二甲苯属于不饱和烃 |