题目内容
请仔细阅读以下转化关系.
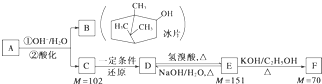
A是从蛇床子果实中提取的一种中草药有效成分,是由碳、氢、氧元素组成的酯类化合物;
B称作冰片,可用于医药和制香精、樟脑等;C的核磁共振氢谱显示其分子中含有4种氢原子;
D中只含一个氧原子,与Na反应放出H2;F为烃.
请回答:(1)B的分子式为 .
(2)B不能发生的反应是(填序号) .
a.氧化反应 b.聚合反应c.消去反应 d.取代反应e.与Br2加成反应
(3)写出D→E、E→F的反应类型:D→E 、E→F .
(4)F的分子式为 .化合物H是F的同系物,相对分子质量为56,写出H所有可能的结构: .
(5)写出A、C的结构简式并用系统命名法给F命名:A: 、C: ;F的名称: .
(6)写出E-→D的化学方程式: .

A是从蛇床子果实中提取的一种中草药有效成分,是由碳、氢、氧元素组成的酯类化合物;
B称作冰片,可用于医药和制香精、樟脑等;C的核磁共振氢谱显示其分子中含有4种氢原子;
D中只含一个氧原子,与Na反应放出H2;F为烃.
请回答:(1)B的分子式为
(2)B不能发生的反应是(填序号)
a.氧化反应 b.聚合反应c.消去反应 d.取代反应e.与Br2加成反应
(3)写出D→E、E→F的反应类型:D→E
(4)F的分子式为
(5)写出A、C的结构简式并用系统命名法给F命名:A:
(6)写出E-→D的化学方程式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:F为烃,相对分子质量为70,则分子中C原子最大数目为
=5…10,则F的分子式是C5H10.由D→E→F的转化可知,E为溴代烃,结合E、F的相对分子质量可知,E脱去1分子HBr发生消去反应生成F,故E分子中含有1个Br原子,E发生水解反应生成D,D为醇,且只含一个氧原子,故D为一元醇,C发生还原反应生成D,C、D、E、F含有相同碳原子数目,即均含有5个碳原子,A为酯类,水解生成C与B,可知C为羧酸,由于D为一元醇,故C为一元羧酸,Mr(C)=102,C的核磁共振氢谱显示其分子中含有4种氢原子,所以C为(CH3)2CHCH2COOH,则D为(CH3)2CHCH2CH2OH、E为(CH3)2CHCH2CH2Br、F为(CH3)2CHCH=CH2,故A为 ,据此解答.
,据此解答.
| 70 |
| 12 |
 ,据此解答.
,据此解答.解答:
解:F为烃,相对分子质量为70,则分子中C原子最大数目为
=5…10,则F的分子式是C5H10.由D→E→F的转化可知,E为溴代烃,结合E、F的相对分子质量可知,E脱去1分子HBr发生消去反应生成F,故E分子中含有1个Br原子,E发生水解反应生成D,D为醇,且只含一个氧原子,故D为一元醇,C发生还原反应生成D,C、D、E、F含有相同碳原子数目,即均含有5个碳原子,A为酯类,水解生成C与B,可知C为羧酸,由于D为一元醇,故C为一元羧酸,Mr(C)=102,C的核磁共振氢谱显示其分子中含有4种氢原子,所以C为(CH3)2CHCH2COOH,则D为(CH3)2CHCH2CH2OH、E为(CH3)2CHCH2CH2Br、F为(CH3)2CHCH=CH2,故A为 ,
,
(1)根据B结构式可知得其分子式为C10H18O,故答案为:C10H18O;
(2)B属于有机物且含有醇羟基,连接醇羟基的碳原子相邻的碳原子上含有氢原子,所以B能发生氧化反应、消去反应、取代反应,因为没有碳碳双键或三键所以不能发生聚合反应、加成反应,故选:be;
(3)D→E反应D中的醇羟基被溴原子取代生成溴代烃,属于取代反应,E→F反应中E中的羟基和氢原子生成水,同时生成碳碳双键,发生的反应属于消去反应,故答案为:取代反应、消去反应;
(4)通过以上分析知,F分子式是C5H10,化合物H是F的同系物,相对分子质量为56,所以H是丁烯,丁烯有碳链异构和顺反异构,所以丁烯的结构简式分别为:CH2=CHCH2CH3、CH2=C(CH3)2、 ,
, ,
,
故答案为:CH2=CHCH2CH3、CH2=C(CH3)2、 、
、 ;
;
(5)由上述分析可知,A的结构简式为 ,C的结构简式为(CH3)2CHCH2COOH,F结构简式为(CH3)2CHCH=CH2,名称为:3-甲基-1-丁烯,
,C的结构简式为(CH3)2CHCH2COOH,F结构简式为(CH3)2CHCH=CH2,名称为:3-甲基-1-丁烯,
故答案为: ;(CH3)2CHCH2COOH;3-甲基-1-丁烯;
;(CH3)2CHCH2COOH;3-甲基-1-丁烯;
(6)E→D是加热条件下,溴代烃和氢氧化钠的水溶液发生取代反应生成醇和溴化钠,所以其反应方程式为: ,
,
故答案为: .
.
| 70 |
| 12 |
 ,
,(1)根据B结构式可知得其分子式为C10H18O,故答案为:C10H18O;
(2)B属于有机物且含有醇羟基,连接醇羟基的碳原子相邻的碳原子上含有氢原子,所以B能发生氧化反应、消去反应、取代反应,因为没有碳碳双键或三键所以不能发生聚合反应、加成反应,故选:be;
(3)D→E反应D中的醇羟基被溴原子取代生成溴代烃,属于取代反应,E→F反应中E中的羟基和氢原子生成水,同时生成碳碳双键,发生的反应属于消去反应,故答案为:取代反应、消去反应;
(4)通过以上分析知,F分子式是C5H10,化合物H是F的同系物,相对分子质量为56,所以H是丁烯,丁烯有碳链异构和顺反异构,所以丁烯的结构简式分别为:CH2=CHCH2CH3、CH2=C(CH3)2、
 ,
, ,
,故答案为:CH2=CHCH2CH3、CH2=C(CH3)2、
 、
、 ;
;(5)由上述分析可知,A的结构简式为
 ,C的结构简式为(CH3)2CHCH2COOH,F结构简式为(CH3)2CHCH=CH2,名称为:3-甲基-1-丁烯,
,C的结构简式为(CH3)2CHCH2COOH,F结构简式为(CH3)2CHCH=CH2,名称为:3-甲基-1-丁烯,故答案为:
 ;(CH3)2CHCH2COOH;3-甲基-1-丁烯;
;(CH3)2CHCH2COOH;3-甲基-1-丁烯;(6)E→D是加热条件下,溴代烃和氢氧化钠的水溶液发生取代反应生成醇和溴化钠,所以其反应方程式为:
 ,
,故答案为:
 .
.
点评:本题考查了有机物的推断,关键确定F的分子式,根据反应条件,采用正推法与逆推法相结合的方法进行推断,需要学生熟练掌握官能团的性质与转化,(4)注意有机物的同分异构体不仅包含碳链异构、官能团异构还包含顺反异构,学生容易忽略顺反异构,为易错点、难点,难度中等.

练习册系列答案
相关题目
下列关于氧化还原反应的叙述中,正确的是( )
| A、氧化还原反应的实质是元素化合价发生了变化 |
| B、氧化剂被还原,还原剂被氧化;氧化剂具有氧化性,还原剂具有还原性 |
| C、得到电子的物质被氧化,失去电子的物质被还原 |
| D、氧化还原反应中,氧化剂和还原剂一定是两种物质 |
某中性有机物C8H16O2在稀硫酸作用下加热得到M和N两种物质,N经氧化最终可得到M,则该中性有机物的结构可能有( )
| A、1种 | B、2种 | C、3种 | D、4种 |