题目内容
18.下列微粒中,属于阳离子的是( )| A. | 11个质子,12个中子,10个电子 | B. | 18个质子,22个中子,18个电子 | ||
| C. | 16个质子,16个中子,18个电子 | D. | 17个质子,18个中子,17个电子 |
分析 原子中质子带正电荷,核外电子带负电荷,如粒子中质子数大于电子数,则为阳离子,以此解答该题.
解答 解:如为阳离子,则质子数大于电子数,只有A符合,B、D中质子数=电子数,为分子或原子,C中质子数少于电子数,为银离子,
故选A.
点评 本题考查元素的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握原子的构成特点,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.某学生的实验报告所列出的下列数据中合理的是 ( )(填写序号).
| A. | 用托盘天平称量25.20g NaCl | |
| B. | 用10mL量筒量取7.1mL稀盐酸 | |
| C. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| D. | 用浓度分别为0.50mol/L,体积各为50mL盐酸、氢氧化钠溶液测定中和热 |
9.1gH2燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式正确的是( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=-142.9kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O (g)△H=-571.6kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O (l)△H=+571.6kJ•mol-1 |
6.1摩单质碳在二氧化碳和氧气的混合气体中高温燃烧,生成气体的物质的量可能是( )
| A. | 2摩 | B. | 2.5摩 | C. | 1.5摩 | D. | 3摩 |
13.水杨酸是重要的精细化工原料,它的结构简式如图.则水杨酸的芳香族同分异构体( )
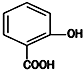

| A. | 可能含有两个醛基 | B. | 可能含有三个羟基 | ||
| C. | 都能与氢氧化钠溶液反应 | D. | 分子式都是C7H6O3 |
3.同温同压下,甲容器内充满了H2气体,乙容器内充满了NH3气体,如果两者氢原子个数相等,则这两个容器的体积比为( )
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 3:1 |
10.表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明.
(1)已知碘在碘酸钾中的化合价为+5,1mol碘酸钾中共含5mol原子,则碘酸钾的化学式为KIO3.
(2)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式:
KIO3+5KI+3H2SO4-3K2SO4+3I2+3H2O
(3)要使上述反应生成的I2从溶液中分离出来,某学生设计如下的操作步骤:
A.检验分液漏斗活塞和上口的玻璃塞是否检漏;
B.把10mL碘水和4mL有机溶剂加入分液漏斗中,并盖好玻璃塞;
C.充分振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
D.把盛有溶液的分液漏斗放在铁架台的铁圈中;
E.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
F.静置
G.旋开活塞,用烧杯接收下层I2的有机溶液;
H.从分液漏斗上口倒出上层液体;
①补全上述操作A检漏C充分振荡 F静置②该实验中用的萃取剂是四氯化碳
③从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏(填操作名称)
(4)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是不稳定,受热易分解.
(5)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为I2+2KClO3=2KIO3+Cl2.
| 配 料 | 氯化钠、碘酸钾 |
| 含碘量 | (20mg~40mg)/1kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、防潮 |
(2)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式:
KIO3+5KI+3H2SO4-3K2SO4+3I2+3H2O
(3)要使上述反应生成的I2从溶液中分离出来,某学生设计如下的操作步骤:
A.检验分液漏斗活塞和上口的玻璃塞是否检漏;
B.把10mL碘水和4mL有机溶剂加入分液漏斗中,并盖好玻璃塞;
C.充分振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
D.把盛有溶液的分液漏斗放在铁架台的铁圈中;
E.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
F.静置
G.旋开活塞,用烧杯接收下层I2的有机溶液;
H.从分液漏斗上口倒出上层液体;
①补全上述操作A检漏C充分振荡 F静置②该实验中用的萃取剂是四氯化碳
③从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏(填操作名称)
(4)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是不稳定,受热易分解.
(5)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为I2+2KClO3=2KIO3+Cl2.
7.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构.则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | |
| B. | 原子序数 d>c>b>a | |
| C. | 离子半径 C>D>B>A | |
| D. | 原子结构的最外层电子数目 A>B>D>C |
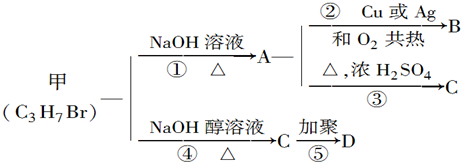
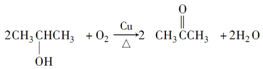

 .
.