题目内容
1.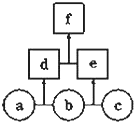 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )| A. | d和e分子中所有原子都不满足8电子结构 | |
| B. | 单质c的氧化性强于单质a | |
| C. | 相同状况下,单质c、a、b的沸点逐渐减小 | |
| D. | f可电离生成两种含10个电子的离子 |
分析 a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,则b一定为氢气,分子中所含原子个数:d>e,f为离子化合物,因此f一定为铵盐,则a是氮气,c为氟气,d是氨气,e为HF,f为NH4F,据此解答.
解答 解:a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,则b一定为氢气,分子中所含原子个数:d>e,f为离子化合物,因此f一定为铵盐,则a是氮气,c为氟气,d是氨气,e为HF,f为NH4F,
A.d是NH3,e为HF,d和e分子中H原子都不满足8电子结构,N、F满足8电子结构,故A错误;
B.a是氮气,c为氟气,单质c的氧化性强于单质a,故B正确;
C.相对分子质量越大,单质的沸点越高,则相同状况下,单质c、a、b的沸点逐渐减小,故C正确;
D.NH4F电离出F-和NH4+,为含10个电子的离子,故D正确,
故选A.
点评 本题考查无机物推断、元素周期律应用等,10电子的d、e生成离子化合物f是推断突破口,难度不大,注意非金属元素形成的离子化合物一定是铵盐,注意对基础知识掌握.

练习册系列答案
相关题目
16.某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,设计如下原电池,盐桥中装有用饱和Na2SO4溶液浸泡过的琼脂.下列说法正确的是( )

| A. | b电极上发生的反应:Fe2+-e-═Fe3+ | |
| B. | a电极上发生氧化反应:MnO4-+8H++5e-═Mn2++4H2O | |
| C. | 外电路电子的流向是从a到b | |
| D. | 电池工作时,盐桥中的SO42-移向甲烧杯 |
10.下列元素中,化学性质最活泼的是( )
| A. | 硅 | B. | 磷 | C. | 硫 | D. | 氯 |
 .
.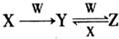 已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.
已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.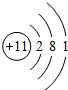 ,用电子式写出C和E形成化合物的过程
,用电子式写出C和E形成化合物的过程 ,用电子式写出A和B形成化合物的过程
,用电子式写出A和B形成化合物的过程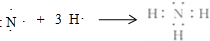 .
.
 .
.