题目内容
12.某有机物4.4g充分燃烧生成8.8g二氧化碳和3.6g水,这种有机物蒸气的密度是相同条件下氢气的22倍,该有机物的分子式是C2H4O.分析 有机物的蒸气密度是相同状况下氢气的22倍,则该有机物的相对分子质量=22×2=43,计算有机物、二氧化碳、水的物质的量,根据原子守恒计算分子中C、H原子数目,再结合相对分子质量确定氧原子数目,进而确定分子式.
解答 解:有机物的蒸气密度是相同状况下氢气的22倍,则该有机物的相对分子质量=22×2=44,
4.4g有机物的物质的量=$\frac{4.4g}{44g/mol}$=0.1mol、CO2的物质的量=$\frac{8.8g}{44g/mol}$=0.2mol、H2O的物质的量=$\frac{3.6g}{18g/mol}$=0.2mol,
根据原子守恒可知,有机物分子中C原子数目=$\frac{0.2mol}{0.1mol}$=2、H原子数目=$\frac{0.2mol×2}{0.1mol}$=4,故O原子数目=$\frac{44-12×2-4}{16}$=1,故该有机物分子式为C2H4O,
故答案为:C2H4O.
点评 本题考查有机物分子式确定,关键是计算有机物的相对分子质量,掌握燃烧法利用原子守恒确定有机物分子式.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
2.同周期ⅡA族元素和ⅢA族元素,它们的原子序数原子序数之差不可能为( )
| A. | 1 | B. | 10 | C. | 11 | D. | 25 |
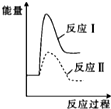
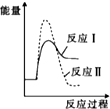
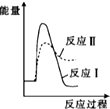
3.下列说法正确的是( )
| A. | 物质发生化学反应时都伴随着能量变化,伴随着能量变化的物质变化一定是化学变化 | |
| B. | 需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 | |
| C. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| D. | 因为石墨变成金刚石吸热,所以金刚石比石墨稳定 |
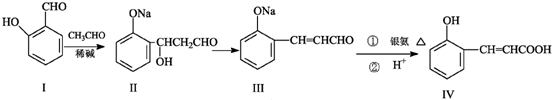
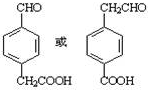
7.在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”.凡具有一个手性碳原子的化合物一定具有光学活性.例如,有机物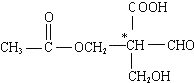 含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
 含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )| A. | 与NaOH溶液共热 | B. | 与银氨溶液共热 | ||
| C. | 与金属钠反应 | D. | 与氢气发生加成反应 |
17.质量数为A,核内中子数为N的R2+离子与16O所形成的Wg氧化物中所含质子的物质的量为( )
| A. | $\frac{W}{A+16}$(A-N+8)mol | B. | $\frac{W}{A+16}$(A-N+10)mol | C. | (A-N+8)mol | D. | $\frac{W}{A}$(A-N+6)mol |
1.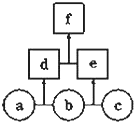 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )| A. | d和e分子中所有原子都不满足8电子结构 | |
| B. | 单质c的氧化性强于单质a | |
| C. | 相同状况下,单质c、a、b的沸点逐渐减小 | |
| D. | f可电离生成两种含10个电子的离子 |
2.在一定条件下,对于A2(g)+3B2(g)?2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最快的是( )
| A. | v(A2)=0.8 mol•L-1•s-1 | B. | v(A2)=30 mol•L-1•min-1 | ||
| C. | v(AB3)=1.0 mol•L-1•s-1 | D. | v(B2)=1.2 mol•L-1•s-1 |

 .
.