题目内容
17.将铜和碳的混合物在空气中充分灼烧,混合物的质量在冷却后没有变化,则原混合物中铜和碳的质量比为( )| A. | 1:1 | B. | 1:4 | C. | 4:1 | D. | 无法确定 |
分析 加热反应后所发生的反应为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO(固体质量增加),C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2(固体质量减少),由题意可知,生成的黑色物质与原混合物的质量相等,即原来的铜、碳混合物变成了CuO,根据质量守恒定律结合题给条件分析,可以知道参加反应氧气的质量与原混合物中碳的质量相等,可以据此解答该题.
解答 解:由题意可知:氧化铜中氧元素的质量等于原混合物中炭粉的质量,因此原混合物中铜粉与碳粉的质量比就是氧化铜中铜元素和氧元素的质量之比,即原混合物中铜和碳的质量比=64:16=4:1.
故选C.
点评 本题考查化学方程式的计算,题目难度不大,明确发生反应的实质为解答关键,试题侧重考查学生运用质量守恒定律分析和解决问题的能力,增强了学生分析问题、整合知识的能力.

练习册系列答案
相关题目
7.下列说法正确的是( )
| A. | 苯酚显酸性,是因为羟基对苯环影响的结果 | |
| B. | 分子式为C2H4和C3H6的物质一定互为同系物 | |
| C. | 聚合物  是苯酚和甲醛在一定条件下反应得到的高分子化合物 是苯酚和甲醛在一定条件下反应得到的高分子化合物 | |
| D. | 1mol 与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH 与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH |
8.下列硫化物中不能直接用金属单质和硫单质反应制得的是( )
| A. | CuS | B. | FeS | C. | ZnS | D. | MgS |
5.下列说法正确的是( )
| A. | 冰的晶体中每个水分子可与周围两个水分子形成氢键 | |
| B. | 手性碳原子不一定是饱和碳原子 | |
| C. | 区分晶体与非晶体最科学的方法是X-射线衍射法 | |
| D. | 晶体中有阳离子就一定有阴离子 |
12.某无色气体可能含有甲烷、一氧化碳、氢气中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全):
①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
| A. | 该气体可能只含有一氧化碳、氢气 | B. | 该气体可能只含有甲烷、一氧化碳 | ||
| C. | 该气体一定只含有甲烷 | D. | 该气体一定只含有甲烷、氢气 |
2.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 实现化石燃料清洁利用,就无需开发新能源 | |
| B. | 垃圾是放错地方的资源,应分类回收利用 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
9.常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是( )
| A. | C2H5OH | B. | CH4 | C. | C2H4O | D. | C3H8 |
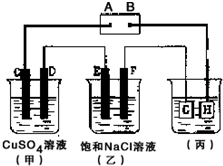 如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题:
如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题: