题目内容
7.下列说法正确的是( )| A. | 苯酚显酸性,是因为羟基对苯环影响的结果 | |
| B. | 分子式为C2H4和C3H6的物质一定互为同系物 | |
| C. | 聚合物  是苯酚和甲醛在一定条件下反应得到的高分子化合物 是苯酚和甲醛在一定条件下反应得到的高分子化合物 | |
| D. | 1mol 与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH 与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH |
分析 A.苯环影响酚-OH;
B.C3H6可能为烯烃或环丙烷;
C. 为酚醛树脂;
为酚醛树脂;
D.2个酚-OH、-个-COOC-及水解生成的酚-OH均与NaOH反应.
解答 解:A.苯酚显酸性,是因为苯环影响酚-OH,故A错误;
B.C3H6可能为烯烃或环丙烷,而C2H4为乙烯,不一定为同系物,故B错误;
C. 为酚醛树脂,为苯酚和甲醛在一定条件下反应得到的高分子化合物,故C正确;
为酚醛树脂,为苯酚和甲醛在一定条件下反应得到的高分子化合物,故C正确;
D.2个酚-OH、-个-COOC-及水解生成的酚-OH均与NaOH反应,则1mol与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH,故D正确;
故选CD.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
18.某化学科学探究活动小组进行了下列实验探究:
Ⅰ、某实验室的废液经测定其主要含有乙醇,此外还有丙酮、乙酸和乙酸乙酯.以上各物质的沸点如下:
现拟通过下列步骤回收乙醇和乙酸:①向废液中加入烧碱溶液,调整溶液的pH=10;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加入浓硫酸(过量),然后再放入耐酸蒸馏器中进行蒸馏,收集馏出物,请回答下列问题:
(l)加入烧碱使溶液的 pH=10的目的是使乙酸乙酯充分水解,中和乙酸
(2)在70℃~85℃时馏出物的主要成分为乙醇
(3)在步骤④中加入过量的浓硫酸的目的是(用化学方程式表示)2CH3COONa+H2SO4(浓)→Na2SO4+2CH3COOH
(4)最后蒸馏的温度控制在85℃~125℃之间,经过一段时间后,蒸馏瓶内残留液中溶质的主要成分是硫酸钠、硫酸.
Ⅱ.为探究苯与液溴发生反应的原理,用如图装置进行实验.(夹持装置已略去)

已知:苯与液溴的反应是放热反应.
根据相关知识回答下列问题:
(1)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始.则Ⅱ中的有机物所发生反应的化学方程式为:
(2)仪器A的名称为:冷凝管.整套实验装置中能防止倒吸的装置有III和IV(填装置序号).
(3)反应结束后,开启K2,关闭K1和分液漏斗活塞,使装置I中的水倒吸入装置Ⅱ中,这样操作的目的是反应结束后装置II中存在大量的溴化氢,使I的水倒吸入II中可以除去溴化氢气体,以免逸出污染空气.
(4)反应结束后,为了得到较纯净的溴苯,对Ⅱ中的溶液按下列步骤分离提纯:
①依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是:除去溴苯中溶有的HBr和Br2
②洗涤后再干燥,即得到粗溴苯,此粗溴苯中还含有的主要杂质为苯,要进一步提纯,下列操作中必须的是C(填入正确选项前的字母):
A、重结晶 B、过滤 C、蒸馏 D、萃取
(5)此装置是否能判断苯与溴发生的是取代反应:是,Ⅲ中的广口瓶中出现淡黄色沉淀
(填“是”则写出能说明发生的是取代反应的现象,填“否”则解释其原因.)
Ⅰ、某实验室的废液经测定其主要含有乙醇,此外还有丙酮、乙酸和乙酸乙酯.以上各物质的沸点如下:
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
(l)加入烧碱使溶液的 pH=10的目的是使乙酸乙酯充分水解,中和乙酸
(2)在70℃~85℃时馏出物的主要成分为乙醇
(3)在步骤④中加入过量的浓硫酸的目的是(用化学方程式表示)2CH3COONa+H2SO4(浓)→Na2SO4+2CH3COOH
(4)最后蒸馏的温度控制在85℃~125℃之间,经过一段时间后,蒸馏瓶内残留液中溶质的主要成分是硫酸钠、硫酸.
Ⅱ.为探究苯与液溴发生反应的原理,用如图装置进行实验.(夹持装置已略去)

已知:苯与液溴的反应是放热反应.
根据相关知识回答下列问题:
(1)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始.则Ⅱ中的有机物所发生反应的化学方程式为:

(2)仪器A的名称为:冷凝管.整套实验装置中能防止倒吸的装置有III和IV(填装置序号).
(3)反应结束后,开启K2,关闭K1和分液漏斗活塞,使装置I中的水倒吸入装置Ⅱ中,这样操作的目的是反应结束后装置II中存在大量的溴化氢,使I的水倒吸入II中可以除去溴化氢气体,以免逸出污染空气.
(4)反应结束后,为了得到较纯净的溴苯,对Ⅱ中的溶液按下列步骤分离提纯:
①依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是:除去溴苯中溶有的HBr和Br2
②洗涤后再干燥,即得到粗溴苯,此粗溴苯中还含有的主要杂质为苯,要进一步提纯,下列操作中必须的是C(填入正确选项前的字母):
A、重结晶 B、过滤 C、蒸馏 D、萃取
(5)此装置是否能判断苯与溴发生的是取代反应:是,Ⅲ中的广口瓶中出现淡黄色沉淀
(填“是”则写出能说明发生的是取代反应的现象,填“否”则解释其原因.)
15.下列说法正确的是( )
| A. | Cu和浓硫酸在加热的条件下可以反应,体现浓硫酸的强氧化性和酸性 | |
| B. | 将SO2通入盛有品红溶液的试管中红色褪去,给试管加热无明显变化 | |
| C. | 将干燥的Cl2通入装有红色鲜花的试管中,红花褪色,说明Cl2具有漂白性 | |
| D. | 将蘸有浓氨水和浓硫酸的玻璃棒靠近,会产生白烟 |
2.下列实验装置或操作不符合实验要求的是( )
| A. |  石油分馏 | B. | 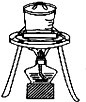 灼烧干海带 | ||
| C. |  用CCl4提取碘水中的碘 | D. | 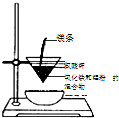 冶炼金属铁 |
12.短周期主族元素X、Y、Z、W原子序数依次增大,X是非金属性最强的元素,在元素周期表中Y位于第IA族,Z的简单离子半径是同周期最小的,W与X属于同一主族.下列说法正确的是( )
| A. | 元素X、Y的简单离子具有相同的电子层结构 | |
| B. | 由Z、W两种元素组成的化合物是离子化合物 | |
| C. | W的简单气态氢化物的热稳定性比X的强 | |
| D. | 离子半径:r(X)<r(Y)<r(Z)<r(W) |
19.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | 热稳定性:HF>H2O>NH3 | B. | 原子半径:F>O>N | ||
| C. | 沸点:乙烷>戊烷>丁烷 | D. | 酸性:H2SO4>H3PO4>HClO4 |
17.将铜和碳的混合物在空气中充分灼烧,混合物的质量在冷却后没有变化,则原混合物中铜和碳的质量比为( )
| A. | 1:1 | B. | 1:4 | C. | 4:1 | D. | 无法确定 |
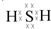 、
、 .
.