题目内容
在标准状况下,1mol二氧化碳的体积约为( )
| A、28L | B、11.2L |
| C、22.4L | D、5.6L |
考点:物质的量的相关计算
专题:计算题
分析:标况下,气体摩尔体积为22.4L/mol,根据V=nVm确定气体体积大小.
解答:
解:标况下,气体摩尔体积为22.4L/mol,1mol二氧化碳气体体积V=nVm=1mol×22.4L/mol=22.4L,
故选C.
故选C.
点评:本题考查了气体体积的计算,根据公式来分析解答即可,注意气体摩尔体积受温度和压强影响,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的离子方程式表示正确的是( )
| A、澄清石灰水中通入过量二氧化碳:OH-+CO2═HCO3- |
| B、铜片跟三氯化铁溶液反应:Fe3++Cu═Cu2++Fe2+ |
| C、漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| D、Fe3O4与稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
下列离子方程式正确的是( )
| A、铝与稀盐酸反应 Al+2H+=Al3++H2↑ |
| B、三氯化铁溶液与氢氧化钠溶液反应 FeCl3+3OH-=Fe(OH)3↓+3Cl- |
| C、用氢氧化钠溶液吸收多余的Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
| D、二氧化碳与石灰水反应 CO2+2OH-=CO32-+H2O |
下列说法正确的是( )
| A、同温同压下甲烷和氧气的密度之比为2:1 |
| B、1 g甲烷和1 g氧气的原子数之比为5:1 |
| C、等物质的量的甲烷和氧气的质量之比为2:1 |
| D、在标准状况下等质量的甲烷和氧气的体积之比为1:2 |
将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A、铁恰好将Fe3+全部还原 |
| B、往反应后溶液中滴入KSCN溶液,不显红色 |
| C、溶液变为浅绿色 |
| D、Fe2+和Fe3+物质的量之比为6:1 |
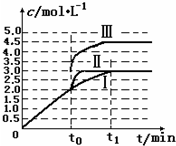 碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.
碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.