题目内容
根据相关的化学原理,下列判断正确的是( )
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于磷化氢的相对分子质量比氨气的大,所以沸点:PH3>NH3 |
| C、若A2+2D-═2A-+D2,则氧化性D2>A2 |
| D、若R2-和M+的电子层结构相同,则离子半径R2->M+ |
考点:氢键的存在对物质性质的影响,微粒半径大小的比较,氧化性、还原性强弱的比较
专题:氧化还原反应专题,化学键与晶体结构
分析:A.氢化物的稳定性与共价键有关;
B.氨气分子间存在氢键,沸点较高;
C.反应中氧化剂的氧化性大于氧化产物的氧化性;
D.R2-和M+的电子层结构相同,则核外电子数相同,阳离子电子数=质子数-所带电荷数,阴离子电子数=质子数+所带电荷数;核外电子排布相同,质子数越大,离子半径越小.
B.氨气分子间存在氢键,沸点较高;
C.反应中氧化剂的氧化性大于氧化产物的氧化性;
D.R2-和M+的电子层结构相同,则核外电子数相同,阳离子电子数=质子数-所带电荷数,阴离子电子数=质子数+所带电荷数;核外电子排布相同,质子数越大,离子半径越小.
解答:
解:A.氢化物的稳定性与共价键有关,共价键的键能越大,氢化物越稳定,氢化物的稳定性与氢键无关,故A错误;
B.氨气分子间存在氢键,沸点较高,则沸点:PH3<NH3,故B错误;
C.反应中氧化剂的氧化性大于氧化产物的氧化性,若A2+2D-═2A-+D2,则氧化性D2<A2,故C错误;
D.R2-和M+的电子层结构相同,则核外电子数相同,则质子数:R>M;核外电子排布相同,质子数越大,离子半径越小,则离子半径R2->M+,故D正确.
故D正确.
B.氨气分子间存在氢键,沸点较高,则沸点:PH3<NH3,故B错误;
C.反应中氧化剂的氧化性大于氧化产物的氧化性,若A2+2D-═2A-+D2,则氧化性D2<A2,故C错误;
D.R2-和M+的电子层结构相同,则核外电子数相同,则质子数:R>M;核外电子排布相同,质子数越大,离子半径越小,则离子半径R2->M+,故D正确.
故D正确.
点评:本题考查了化学键、氢键、氧化性比较、离子半径的比较等,题目难度不大,侧重于基础知识的考查,注意对有关知识的积累.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
化学知识在日常生活中有很多应用,下列说法正确的是( )
| A、用食盐清洗热水瓶中的水垢 |
| B、漂白粉在空气中容易变质的原因是Ca(ClO)2见光分解 |
| C、加碘食盐,能使淀粉显蓝色 |
| D、氯水应避光保存,是因为HClO见光分解 |
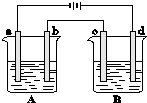 如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )
如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )| A、1:1:2:1 |
| B、2:1:1:1 |
| C、2:2:4:1 |
| D、2:1:2:1 |
NA代表阿伏加德罗常数,下列有关叙述错误的是( )
| A、1mol 固体NaHSO4含有的阴阳离子总数为2NA |
| B、标准状况下22.4L CH4和C2H4的混合气体所含氢原子数为4NA |
| C、常温常压下,3.4gNH3中含N-H键数目为0.6NA |
| D、56 g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA |
下列说法正确的是( )
| A、CO2的相对分子质量为44g/mol |
| B、“物质的量”是“物质的质量”的简称 |
| C、摩尔只能用于计量纯净物 |
| D、阿伏伽德罗常数的单位是mol-1 |
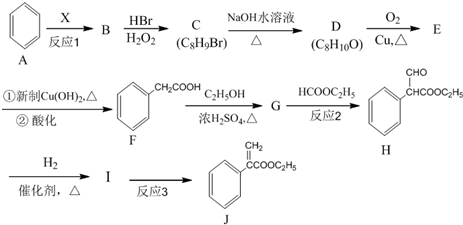
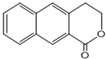 是一种重要的药物合成中间体,请结合题目所给信息,写出以
是一种重要的药物合成中间体,请结合题目所给信息,写出以 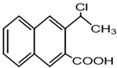 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2