题目内容
在标准状况下,由排空气法收集一瓶氯化氢气体,测得烧瓶内气体对氢气的相对密度为17,现将烧瓶倒立于水中,则进入烧瓶中水的体积占烧瓶容积的几分之几?若溶质不扩散,烧瓶内溶液的物质的量浓度是多少?
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:溶液上升体积等于HCl的体积,根据相对氢气的密度计算集气瓶内气体的平均相对分子质量,进而计算HCl的体积分数;
令HCl的体积为VL,根据n=
计算HCl物质的量,再根据c=
计算溶液物质的量浓度.
令HCl的体积为VL,根据n=
| V |
| Vm |
| n |
| V |
解答:
解:集气瓶内气体的平均相对分子质量=17×2=34,令HCl的体积分数为x,则空气的体积分数为(1-x),故36.5x+29(1-x)=34,解得x=
,溶液上升体积等于HCl的体积,故烧瓶内液面上升的体积占烧瓶总体积的
;
令HCl的体积为VL,其物质的量=
=
mol,溶液物质的量浓度=
=0.045mol/L,
答:烧瓶内液面上升的体积占烧瓶总体积的
;所得溶液的物质的量浓度为0.045mol/L.
| 2 |
| 3 |
| 2 |
| 3 |
令HCl的体积为VL,其物质的量=
| VL |
| 22.4L/mol |
| V |
| 22.4 |
| ||
| VL |
答:烧瓶内液面上升的体积占烧瓶总体积的
| 2 |
| 3 |
点评:本题考查物质的量浓度有关计算,关键是根据HCl溶于水确定溶液上升体积等于HCl的体积,注意对公式的理解与灵活应用,难度不大.

练习册系列答案
相关题目
 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容.某同学从该试剂瓶中取出24.0g固体,配成一定体积的溶液,请计算
如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容.某同学从该试剂瓶中取出24.0g固体,配成一定体积的溶液,请计算 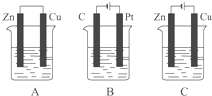 如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液.按要求写出电极反应式.A池中铜电极上的电极反应式为:
如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液.按要求写出电极反应式.A池中铜电极上的电极反应式为: