题目内容
4.8g O2和0.2mol CO2,它们的物质的量之比是 ,质量之比是 ,在同温同压下的体积之比是 .
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据公式m=nM计算物质的量之比和质量之比,根据阿伏加德罗定律可知,同温同压下气体的体积之比等于物质的量之比.
解答:
解:4.8g O2的物质的量n=
=
=0.15mol,和0.2mol CO2,它们的物质的量之比是0.15:0.2=3:4,0.2mol CO2的质量是0.2mol×44g/mol=8.8g,质量之比是4.8:8.8=6:11,在同温同压下的体积之比等于物质的量之比,即为3:4,
故答案为:3:4;6:11;3:4.
| m |
| M |
| 4.8g |
| 32g/mol |
故答案为:3:4;6:11;3:4.
点评:本题考查学生公式m=nM以及阿伏伽德罗定律的应用知识,注意知识的灵活应用是解题的关键,难度中等.

练习册系列答案
相关题目
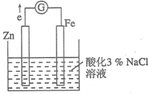 某化学兴趣小组对电化学问题进行了实验探究.利用如图装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生.
某化学兴趣小组对电化学问题进行了实验探究.利用如图装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生.