题目内容
有X、Y、Z、W四种元素,已知:
①它们都是短周期元素,X和Z在同一周期,在常温下W元素的单质是黄绿色气体;
②它们可以组成:X2Z、ZY2、ZY3 化合物;
③ZY3与水化合生成一种强酸,此强酸与X2Z反应可生成一种气体A.根据以上推断,回答下列问题:
(1)X、Y、Z、W四种元素的元素符号依次为: 、 、 、 ;
(2)画出Z2-的结构示意图: ;
(3)A和W元素的单质反应的化学方程式是: ;
(4)W的最高价氧化物溶于水得到一种稀溶液,写出该反应的离子方程式: .
①它们都是短周期元素,X和Z在同一周期,在常温下W元素的单质是黄绿色气体;
②它们可以组成:X2Z、ZY2、ZY3 化合物;
③ZY3与水化合生成一种强酸,此强酸与X2Z反应可生成一种气体A.根据以上推断,回答下列问题:
(1)X、Y、Z、W四种元素的元素符号依次为:
(2)画出Z2-的结构示意图:
(3)A和W元素的单质反应的化学方程式是:
(4)W的最高价氧化物溶于水得到一种稀溶液,写出该反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:有X、Y、Z、W四种元素,它们都是短周期元素,在常温下W元素的单质是黄绿色气体,则W为Cl元素;它们可以组成:X2Z、ZY2、ZY3 化合物,而ZY3与水化合生成一种强酸,应是SO3与水反应生成硫酸,可推知Y为O、Z为S,X和Z在同一周期,由形成的化合物可知X为+1价,则X为Na,硫酸与Na2S反应可生成一种气体A为H2S,以此解答该题.
解答:
解:有X、Y、Z、W四种元素,它们都是短周期元素,在常温下W元素的单质是黄绿色气体,则W为Cl元素;它们可以组成:X2Z、ZY2、ZY3 化合物,而ZY3与水化合生成一种强酸,应是SO3与水反应生成硫酸,可推知Y为O、Z为S,X和Z在同一周期,由形成的化合物可知X为+1价,则X为Na,硫酸与Na2S反应可生成一种气体A为H2S,
(1)由上述分析可知,X、Y、Z、W四种元素的元素符号依次为:Na、O、S、Cl,故答案为:Na;O;S;Cl;
(2)S2-离子核外有18个电子层,有3个电子层,各层电子数为2、8、8,结构示意图为: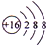 ,故答案为:
,故答案为: ;
;
(3)硫化氢与氯气反应生成S与HCl,化学反应方程式是:H2S+Cl2=S↓+2HCl,故答案为:H2S+Cl2=S↓+2HCl;
(4)W的最高价氧化物为Cl2O7,溶于水得到高氯酸,化学反应方程式为:Cl2O7+H2O=2H++2ClO4-,故答案为:Cl2O7+H2O=2H++2ClO4-.
(1)由上述分析可知,X、Y、Z、W四种元素的元素符号依次为:Na、O、S、Cl,故答案为:Na;O;S;Cl;
(2)S2-离子核外有18个电子层,有3个电子层,各层电子数为2、8、8,结构示意图为:
 ,故答案为:
,故答案为: ;
;(3)硫化氢与氯气反应生成S与HCl,化学反应方程式是:H2S+Cl2=S↓+2HCl,故答案为:H2S+Cl2=S↓+2HCl;
(4)W的最高价氧化物为Cl2O7,溶于水得到高氯酸,化学反应方程式为:Cl2O7+H2O=2H++2ClO4-,故答案为:Cl2O7+H2O=2H++2ClO4-.
点评:本题考查无机物的推断,侧重对化学用语的考查,推断元素是解题关键,注意把握相关物质的性质,难度中等.

练习册系列答案
相关题目
 短周期非金属主族元素X、Y、Z、W在周期表中的相对位置如图,下列说法中,正确的是( )
短周期非金属主族元素X、Y、Z、W在周期表中的相对位置如图,下列说法中,正确的是( )| A、Z的氧化物只有一种 |
| B、Y的最高价氧化物的水化物与其氢化物反应一定生成盐 |
| C、X的单质不可能把Z从其化合物中还原出来 |
| D、一定条件下,W的单质一定能与H2发生化合反应 |
一定温度时,向2.0L恒容密闭容器中充入2mol SO2和1mol O2,发生反应:
2SO2(g)+O2(g)?2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
2SO2(g)+O2(g)?2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
A、反应在前t1 s 的平均速率v(O2)=
| ||
| B、保持其他条件不变,体积压缩到1.0L,平衡常数将增大 | ||
| C、相同温度下,起始时向容器中充入4mol SO3,达到平衡时,SO3的转化率大于10% | ||
D、保持温度不变,向该容器中再充入2mol SO2、1mol O2,反应达到新平衡时
|