题目内容
60 27 |
60 27 |
A Z |
0 -1 |
(1)下列关于
60 27 |
A.质子数是27 B.电子数是27 C.质量数是27 D.中子数是60
(2)在上述衰变方程中,衰变产物Ni的质量数A为
(3)元素的化学性质主要取决于
A.最外层电子数 B.核内中子数 C.核内质子数 D.质量数不同
(4)不同种元素的本质区别是
A.质子数不同 B.中子数不同 C.电子数不同 D.质量数不同.
考点:核素,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:(1)根据6027Co元素符号左下角数字表示质子数,左上角数字表示质量数,质子数+中子数=质量数,原子中质子数=核外电子数来分析解答;
(2)核反应方程的质量数守恒,电荷数守恒,核外的电子数与质子数相等;
(3)元素的化学性质,与原子的最外层电子数关系非常密切,原子的最外层电子少于4个时,容易失去电子;多于4个少于8个时,容易获得电子;最外层为8个电子时,元素的化学性质最稳定.元素的原子的最外层电子数相同的具有相似的化学性质;
(4)元素是具有相同核电荷数(即核内质子数)的一类原子的总称.
(2)核反应方程的质量数守恒,电荷数守恒,核外的电子数与质子数相等;
(3)元素的化学性质,与原子的最外层电子数关系非常密切,原子的最外层电子少于4个时,容易失去电子;多于4个少于8个时,容易获得电子;最外层为8个电子时,元素的化学性质最稳定.元素的原子的最外层电子数相同的具有相似的化学性质;
(4)元素是具有相同核电荷数(即核内质子数)的一类原子的总称.
解答:
解:(1)A.6027Co中质子数为27,故A错误;
B.原子中质子数=核外电子数,6027Co中电子数为27,故B错误;
C.6027Co中质量数为60,故C正确;
D.6027Co中中子数=质量数-质子数=60-27=33,故D正确.
故答案为:CD;
(2)核外电子数等于质子数,所以
Co的核外电子数为27,根据质量数和电荷数守恒知:
Co═
Ni+
e+Ve,A=60,Z=28,故答案为:60;28;
(3)当原子的最外层电子少于4个时,容易失去电子;多于4个少于8个时,容易获得电子;最外层为8个电子时,元素的化学性质最稳定.元素的化学性质主要决定于原子的最外层电子数,故答案为:A;
(4)根据元素的概念,元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的微粒是质子数即元素的最本质区别是质子数不同,故答案为:A.
B.原子中质子数=核外电子数,6027Co中电子数为27,故B错误;
C.6027Co中质量数为60,故C正确;
D.6027Co中中子数=质量数-质子数=60-27=33,故D正确.
故答案为:CD;
(2)核外电子数等于质子数,所以
60 27 |
60 27 |
A Z |
0 -1 |
(3)当原子的最外层电子少于4个时,容易失去电子;多于4个少于8个时,容易获得电子;最外层为8个电子时,元素的化学性质最稳定.元素的化学性质主要决定于原子的最外层电子数,故答案为:A;
(4)根据元素的概念,元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的微粒是质子数即元素的最本质区别是质子数不同,故答案为:A.
点评:本题考查了质子数、质量数、中子数和电子数之间的关系,难度不大,注意阴阳离子中电子数的计算方法,属于基础知识.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A、节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
| B、小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 |
| C、为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 |
| D、面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于过氧化物,过氧化苯甲酰属于有机物 |
下列溶液中,溶质的物质的量浓度为1mol?L-1的是( )
| A、将40g NaOH溶于1L水所得的溶液 |
| B、将0.5mol?L-1的NaNO3溶液100mL加热蒸发掉50g水所得的溶液 |
| C、将23g Na溶于水并配成1L的溶液 |
| D、从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L |
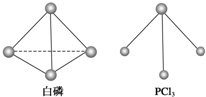 白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10.
白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10.

 锂离子电池是具有电压高、能量密度大、循环性能好等突出优点的高效绿色产品.某锂离子电池的结构如右图所示,以石墨化的碳、氧化钴锂(LiCoO2)为电极,当充电时,阳极上发生的电极反应为LiCoO2-xe-=Li1-xCoO2+xLi+,总反应式为LiCoO2+6C=Li1-xCoO2+LixC6.
锂离子电池是具有电压高、能量密度大、循环性能好等突出优点的高效绿色产品.某锂离子电池的结构如右图所示,以石墨化的碳、氧化钴锂(LiCoO2)为电极,当充电时,阳极上发生的电极反应为LiCoO2-xe-=Li1-xCoO2+xLi+,总反应式为LiCoO2+6C=Li1-xCoO2+LixC6.