题目内容
下列溶液中,溶质的物质的量浓度为1mol?L-1的是( )
| A、将40g NaOH溶于1L水所得的溶液 |
| B、将0.5mol?L-1的NaNO3溶液100mL加热蒸发掉50g水所得的溶液 |
| C、将23g Na溶于水并配成1L的溶液 |
| D、从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:A、c=
中,体积指溶液体积不是溶剂体积;
B、根据溶液100mL加热蒸发掉50g水,溶液密度和水的密度不同,蒸发溶液50g水后溶液体积不是50ml;
C、根据n=
计算溶质物质的量,结合c=
计算浓度判断;
D、根据溶液浓度的均一性判断.
| ||
| V |
B、根据溶液100mL加热蒸发掉50g水,溶液密度和水的密度不同,蒸发溶液50g水后溶液体积不是50ml;
C、根据n=
| m |
| M |
| n |
| V |
D、根据溶液浓度的均一性判断.
解答:
解:A.C=
中,体积指溶液体积不是溶剂体积,所以40gNaOH溶解于1L水中配成的NaOH溶液浓度不是1mol/L,故A错误.
B、将0.5mol?L-1的NaNO3溶液100mL加热蒸发掉50g水,溶液密度和水的密度不同,蒸发溶液50g水后溶液体积不是50ml所得的溶液的物质的量浓度不是1mol/L,故B错误.
C、将23g Na溶于水并配成1L的溶液,溶质物质的量=
=1mol,混合后溶液的物质的量浓度是1mol/L,故C正确;
D、溶液的物质的量浓度有均一性,与取出溶液的体积大小无关,从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为2mol/L,故D错误.
故选C.
| ||
| V |
B、将0.5mol?L-1的NaNO3溶液100mL加热蒸发掉50g水,溶液密度和水的密度不同,蒸发溶液50g水后溶液体积不是50ml所得的溶液的物质的量浓度不是1mol/L,故B错误.
C、将23g Na溶于水并配成1L的溶液,溶质物质的量=
| 23g |
| 23g/mol |
D、溶液的物质的量浓度有均一性,与取出溶液的体积大小无关,从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为2mol/L,故D错误.
故选C.
点评:本题考查了有关物质的量浓度的问题,难度不大,注意溶液的浓度有均一性,与取出溶液的体积大小无关.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、0.1 mol/L的碳酸钠溶液中,Na+和CO32-离子个数比是2:1 |
| B、析氢腐蚀负极发生氧化反应析出氢气,吸氧腐蚀正极发生还原反应吸收氧气 |
| C、向KI溶液中滴加氯水,振荡,静置后能观察到液体会分层,下层呈紫色 |
| D、除去CO2中混有的少量SO2,可将混合气体通通盛有酸性KMnO4溶液的洗气瓶 |
下列反应的离子方程式书写正确的是( )
| A、稀醋酸与氢氧化钠溶液的反应:H++OH-═H2O |
| B、铜粉与稀硝酸的反应:Cu+2H+═Cu2++H2↑ |
| C、氯气与碘化钾溶液的反应:Cl2+I-═Cl-+I2 |
| D、碳酸钠溶液与足量稀盐酸的反应:CO32-+2H+═H2O+CO2↑ |
用如图实验装置和方法进行相应实验,能达到实验目的是( )
A、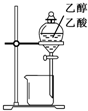 分离乙醇与乙酸 |
B、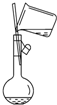 向容量瓶中转移液体 |
C、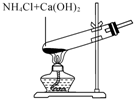 制备少量氨气 |
D、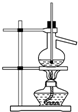 分馏石油 |