题目内容
2.下列有关反应速率说法正确的是( )| A. | C(s)+H2O(g)?CO(g)+H2(g) 加入大量C固体,V正 增大,V逆 减小 | |
| B. | Zn(s)+HCl(aq)═ZnCl2(aq)+H2(g),使用纯锌比粗锌反应速率快 | |
| C. | 对于反应H2(g)+I2(g)?2HI(g),恒温恒容充入Ne,容器内压强增大,V正、V逆 均增大 | |
| D. | 对于反应2SO2(g)+O2(g)═2SO3(g)当升高温度V正、V逆 都加快 |
分析 A.固体量的多少不影响化学反应速率;
B.原电池能加快化学反应速率;
C.恒温恒容条件下充入Ne,容器内压强增大,但参加反应的各物质浓度不变,反应速率不变;
D.升高温度,活化分子百分数增大,正逆反应速率都增大.
解答 解:A.固体量的多少不影响化学反应速率,所以加入大量C固体,正逆反应速率不变,故A错误;
B.原电池能加快化学反应速率,粗锌和稀盐酸能构成原电池,纯锌和稀盐酸不能构成原电池,所以粗锌反应速率大于纯锌,故B错误;
C.恒温恒容条件下充入Ne,容器内压强增大,但参加反应的各物质分压不变、浓度不变,所以反应速率不变,故C错误;
D.升高温度,使部分非活化分子转化为活化分子,所以活化分子百分数增大,正逆反应速率都增大,故D正确;
故选D.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度、温度、压强等因素对化学反应速率影响原理及适用条件是解本题关键,易错选项是C,只有通过改变压强而改变反应物或生成物浓度的才能引起平衡移动,题目难度不大.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- | |
| B. | 含有0.1 mol•L-1Fe3+的溶液中:K+、Mg2+、I-、SO42- | |
| C. | 能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- | |
| D. | c(Al3+)=0.5 mol•L-1的溶液中:Na+、K+、AlO2-、SO42- |
10.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),能说明该可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 体系的压强不再发生变化 | |
| B. | v(CO2)=v(H2O) | |
| C. | 生成n mol CH3OH的同时生成n mol H2O | |
| D. | 3 mol H-H键断裂的同时断裂2 mol H-O键 |
17.实验室用加热固体氯化铵和氢氧化钙的混合物制取氨,反应的化学方程式为:Ca(OH)2+2NH4Cl═CaCl2+2NH3↑+2H2O.所制得气体中常含有少量杂质气体,为了得到纯净的氨气并加以检验,请在下列装置或试剂中,根据要求作出适当选择,并将编号字母填入表中的空格处.
(1)装置:
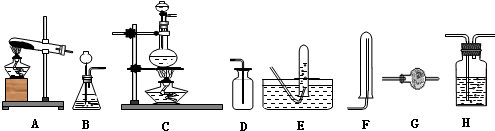
(2)试剂:a.NaOH溶液 b.澄清石灰水 c.浓硫酸 d.饱和NaHCO3溶液
e.碱石灰 f.品红溶液 g.湿润的红色石蕊试纸
(1)装置:

(2)试剂:a.NaOH溶液 b.澄清石灰水 c.浓硫酸 d.饱和NaHCO3溶液
e.碱石灰 f.品红溶液 g.湿润的红色石蕊试纸
| 制取气体 | 杂质气体 | 制取气体的发生装置 | 除去杂质气体的净化装置 | 收集装置 | 净化装置内 所用试剂 | 检验制得气体所用试剂 |
| NH3 | H2O(g) |
14.能源分类相关图如图所示,下列四组选项中,全部符合图中阴影部分的能源是( )
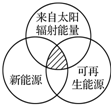

| A. | 沼气、煤炭、石油 | B. | 海洋能、地热能、核能 | ||
| C. | 天然气、水能、生物能 | D. | 风能、太阳能、潮汐能 |
11.下表是几种常见物质的燃烧热.
请回答下列问题:
(1)写出H2燃烧的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol;
(2)1g H2(g)完全燃烧放出的热量大于(填“大于”“小于”或“等于”)1g C(石墨,s)完全燃烧放出的热量.
(3)分解9g液态水制氢气时,吸收的热量为142.9KJ;
(4)1mol C(石墨,s)所具有的总能量低于(填“高于”“低于”“等于”)1mol C(金刚石,s)所具有的总能量,石墨和金刚石中,较稳定的是石墨(填名称).
| 序号 | 名称 | 化学式 | △H(kJ•mol-1) |
| ① | 石墨 | C(s) | -393.5 |
| ② | 金刚石 | C(s) | -395.4 |
| ③ | 氢气 | H2(g) | -285.8 |
(1)写出H2燃烧的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol;
(2)1g H2(g)完全燃烧放出的热量大于(填“大于”“小于”或“等于”)1g C(石墨,s)完全燃烧放出的热量.
(3)分解9g液态水制氢气时,吸收的热量为142.9KJ;
(4)1mol C(石墨,s)所具有的总能量低于(填“高于”“低于”“等于”)1mol C(金刚石,s)所具有的总能量,石墨和金刚石中,较稳定的是石墨(填名称).
20.①花生油和水混合液②39%的乙醇溶液③使浑浊的食盐水变澄清,分离上各混合物的正确方法依次是( )
| A. | 分液、过滤、蒸馏 | B. | 过滤、蒸馏、分液 | C. | 分液、蒸馏、过滤 | D. | 蒸馏、过滤、分液 |
 .
.