题目内容
10.联合生产是实现节能减排的重要措施,工业上合成氨和硝酸的联合生产具有重要意义.如图1是工业上合成氨的简易流程: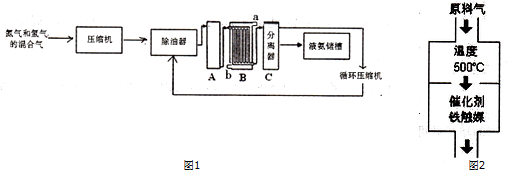
(1)设备A内部结构如图2所示,其名称是合成塔,其中发生的化学反应方程式为N2 +3H2 $?_{催化剂}^{高温、高压}$2NH3 ;选择500℃进行反应的主要原因是此温度下催化剂效率最高;生产中原料气必须进行脱硫,目的是防止催化剂中毒.
(2)设备B的名称是冷却塔或(冷凝器),其作用是利用余热,节约能源,图中a和b是两个通水口,其中入水口是b(填“a”或“b”).
(3)氮气和氢气的混合气体通过压缩机压缩的原因是增大压强,加快反应速率,使平衡朝生成NH3的方向进行.
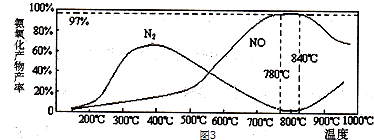
(4)生产出来的NH3可以用来生产硝酸.其中在氨气催化氧化过程中,不同温度下生成产物可能有所不同,温度对氨氧化产物产率的影响如图3所示;当温度大于900℃时,NO的产率下降的主要原因是部分NO转化为N2.
(5)某化肥厂用NH3制备NH4N03.已知:由NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HN03所用NH3的质量占总耗NH3质量(不考虑其它损耗)的54%(保留两位有效数字).
分析 (1)根据图示可知,设备A为合成塔、B为冷凝器或冷凝塔;工业合成氨中合成塔中的反应为氮气和氢气在高温高压条件下生成氨气,据此写出反应的化学方程式;合成氨的反应属于放热反应,根据化学反应速率和平衡移动知识来分析选择500℃的原因;生产中原料气必须进行脱硫,防止催化剂中毒;
(2)B为冷凝器或冷凝塔;作用是利用余热,节约能源;
(3)根据增大压强对平衡移动的影响知识来回答;
(4)由图象可知,温度高于900℃时,NO的产率降低,氮气的产率增大,各反应为放热反应,高温下不利于向正反应进行,应是NO转变为N2所致;
(5)根据氮原子守恒可知,NH3~NO~HNO3,以此计算.
解答 解:(1)合成氨的工业设备是合成塔;N2与H2合成NH3所用的催化剂是铁砂网,温度过低,反应速率较慢,温度较高,不利合成氨气,选择500℃的主原因是在这个温度下催化剂活性最大;生产中原料气必须进行脱硫可以防止催化剂中毒;
故答案为:合成塔,N2 +3H2 $?_{催化剂}^{高温、高压}$ 2NH3 ,此温度下催化剂效率最高,防止催化剂中毒;
(2)B为冷凝器或冷却塔;合成氨的反应属于放热反应,用热交换器可以充分利用余热,节约能源;氮、氢混合气体送入合成塔前要通过压缩机压缩,来增大压强,这样可以加快化学反应速率,还可以让化学平衡朝生成NH3的方向进行;a和b是两个通水口,其中入水口应考虑下进上出;
故答案为:冷却塔或(冷凝器);利用余热,节约能源;b;
(3)增大压强,加快反应速率,平衡向气体体积减小的方向移动,即平衡朝生成NH3的方向进行;
故答案为:增大压强,加快反应速率,使平衡朝生成NH3的方向进行;
(4)各反应为放热反应,高温下不利于向正反应进行,由图象可知,温度高于900℃时,NO的产率降低,氮气的产率增大,故温度高于900℃时应是部分NO转化为N2;
故答案为:部分NO转化为N2;
(5)由NH3制NO的产率是94%、NO制HNO3的产率是89%,根据氮原子守恒可知,NH3~NO~HNO3,则1mol氨气可得到硝酸1mol×94%×89%=0.8366mol,由HNO3+NH3═NH4NO3,则该反应消耗的氨气的物质的量为0.8366mol,氨气的质量之比等于物质的量之比,则制HNO3所用去的NH3的质量占总耗NH3质量的百分数为 $\frac{1mol}{1mol+0.8366mol}$×100%=54%;即制HNO3所用去的NH3的质量占总耗NH3质量的54%;
故答案为:54.
点评 本题考查了工业制备原理应用,流程分析,实验制备物质的分析判断,利用物质的转化及质量守恒的方法来进行简单计算,使用硝酸铵的注意事项,明确转化中的化学反应得出物质之间的关系是解答的关键,题目难度中等.

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案①向溶液中滴加过量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断:该溶液中存在的离子组可能是.
| A. | Al3+、Mg2+、SO32- | B. | K+、CO32-、I- | C. | Al3+、CO32-、I- | D. | Na+、Br-、CO32- |
| I A | II A | III A | IV A | V A | VI A | VII A | 0 | |
| 一 | A | |||||||
| 二 | B | C | D | E | F | |||
| 三 | G | H | I | |||||
| 四 | J |
(1)G元素与E元素形成的化合物的化学式可能是Na2O、Na2O2,I与J的原子序数相差为18.
(2)上述10种元素的最高价氧化物对应的水化物中,碱性最强的是NaOH(用化合物的化学式表示,下同),酸性最强的是HClO4,E、F、G三种元素形成的简单离子半径由大到小的顺序是O2->F->Na+(用离子符号回答).
| A. | 标准状况下,11.2L N2和O2混合气体中所含分子数为0.5NA | |
| B. | 6g SiO2所含分子数为0.1NA,化学键总数为0.4NA | |
| C. | 常温常压下,20g ND3中所含质子数为10NA | |
| D. | 向含0.2mol NH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目为NA |
 溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr$\stackrel{硫酸}{→}$CH3CH2Br+H2O
某课外小组欲在实验室制备溴乙烷的装置如图.数据如下表.
| 物质 数据 | 乙醇 | 溴乙烷 | 1,2-二溴乙烷 | 乙醚 | 浓硫酸 |
| 密度/g•cm-3 | 0.79 | 1.46 | 2.2 | 0.71 | 1.84 |
| 熔点(℃) | -130 | -119 | 9 | -116 | 10 |
| 沸点(℃) | 78.5 | 38.4 | 132 | 34.6 | 338 |
| 在水中的溶解度(g/100g水) | 互溶 | 0.914 | 1 | 7.5 | 互溶 |
(1)加入药品之前须做的操作是:检查装置的气密性,实验进行的途中若发现未加入碎瓷片,其处理的方法是待冷却后重新进行操作.
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是冷凝回流.温度计的温度应控制在38.4℃~78.5℃之间.
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是SO2+2OH-=SO32-+H2O,Br2+2OH-=Br-+BrO-+H2O,此操作可在分液漏斗(填写玻璃仪器名称)中进行,同时进行分离.
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了防止溴化氢气体的挥发.
(5)粗产品中含有的主要有机液体杂质是乙醚,为进一步制得纯净的溴乙烷,对粗产品进行水洗涤、分液,再加入无水CaCl2,进行蒸馏操作.
| A. | BF3 | B. | CO2 | C. | NH3 | D. | PCl5 |
| A. | Y、Z、X | B. | X、Y、Z | C. | X、Z、Y | D. | Z、Y、X |