题目内容
2.下列分子中所有原子都满足最外层为8电子结构的是( )| A. | BF3 | B. | CO2 | C. | NH3 | D. | PCl5 |
分析 在共价化合物中,各元素化合价绝对值+元素原子的最外层电子数=8,则该元素的原子就满足8电子结构,否则不能满足8电子结构,据此进行判断.
解答 解:A.BF3中B元素化合价为+3,B原子最外层电子数为3,所以最外层电子数为:3+3=6,B原子不满足8电子结构,故A错误;
B.CO2中O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构;C原子的族序数+成键数=4+4=8,所以满足所有原子最外层为8电子结构,故B正确;
C.NH3分子中,H原子最外层满足2电子结构,故C错误;
D.PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故D错误;
故选B.
点评 本题考查8电子结构的判断,题目难度不大,明确元素化合价绝对值+元素原子的最外层电子数=8,则该元素原子满足8电子结构是关键,注意离子化合物不适合,试题培养了学生的灵活应用能力.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
15.一定能在下列溶液中大量共存的离子组是( )
| A. | pH=0的溶液:Fe2+、Mg2+、NO3-、SO42- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- | |
| D. | pH=12的溶液:Na+、K+、〔Al(OH)4〕-、CO32- |
16.化学与生产、生活密切相关.下列说法中不正确的是( )
| A. | 从海水中提取食用的精盐,需要有化学反应才能实现 | |
| B. | 高温及常用的消毒剂可使禽流感病毒蛋白质变性 | |
| C. | 生活中的铜制品既能发生析氢腐蚀又能发生吸氧腐蚀 | |
| D. | 植物油中含有碳碳双键,在空气中长时间放置容易氧化变质 |
17.下列关于离子的检验正确的是( )
| A. | 向某溶液中加入足量稀硫酸,无明显现象,再加入AgNO3溶液,出现白色沉淀,则溶液中有Cl- | |
| B. | 向某溶液中滴加浓硫酸,将产生的气体通入品红溶液中,品红褪色,则溶液中一定有SO32- | |
| C. | 用洁净的铂丝蘸取某溶液在无色火焰上灼烧,透过蓝色钴玻璃观察火焰呈紫色,则溶液中有K+ | |
| D. | 在某溶液中,先加入足量BaCl2溶液,有白色沉淀生成;再加入足量稀盐酸,沉淀不溶解,则证明该溶液中含SO42- |
7.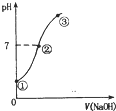 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )| A. | ①点所示溶液中只存在HC1O的电离平衡 | |
| B. | ②到③的过程中水的电离程度一定减少 | |
| C. | ②点处表示氯气与氢氧化钠溶液恰好反应完全 | |
| D. | ②点所示溶液中:c( Na+)=c(C1-)+c(ClO -) |
14.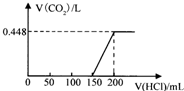 某混合溶液中含有NaOH与Na2CO3,向该溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解).则该混合溶液中NaOH与Na2CO3物质的量之比为( )
某混合溶液中含有NaOH与Na2CO3,向该溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解).则该混合溶液中NaOH与Na2CO3物质的量之比为( )
 某混合溶液中含有NaOH与Na2CO3,向该溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解).则该混合溶液中NaOH与Na2CO3物质的量之比为( )
某混合溶液中含有NaOH与Na2CO3,向该溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解).则该混合溶液中NaOH与Na2CO3物质的量之比为( )| A. | 1:1 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
11.下列离子方程式正确的是( )
| A. | 铝溶解在NaOH溶液中:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑ | |
| B. | 氨水滴入AlCl3溶液中:Al3++3OH-═Al(OH)3↓ | |
| C. | MgO溶于稀盐酸中:O2-+2H+═H2O | |
| D. | Al(OH)3溶于稀硫酸中:OH-+H+═H2O |
12.柠檬烯具有特殊香气.可溶于乙醇或乙醚,不溶于水,其结构简式如图所示: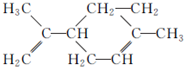 ,有关柠檬烯的说法正确的是( )
,有关柠檬烯的说法正确的是( )
 ,有关柠檬烯的说法正确的是( )
,有关柠檬烯的说法正确的是( )| A. | 柠檬烯分子为非极性分子 | |
| B. | 柠檬烯分子中所有碳原子处于同一个平面上 | |
| C. | 柠檬烯能与酸性高锰酸钾溶液发生取代反应 | |
| D. | 柠檬烯的分子式为C10H16,能使溴的四氯化碳溶液褪色 |