题目内容
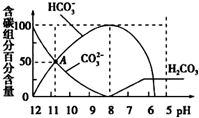 常温下,在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L 盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.下列说法不正确的是( )
常温下,在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L 盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.下列说法不正确的是( )| A、0.1 mol/L Na2CO3溶液中c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
| B、在A点:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| C、常温下CO2饱和溶液的pH约为5.6 |
| D、当加入20 mL盐酸时,混合溶液的pH约为8 |
考点:离子浓度大小的比较
专题:
分析:A.根据溶液的电荷守恒判断;
B.由图象可知,A点c(HCO3-)=c(CO32-),溶液呈碱性,则c(OH-)>c( H+);
C.pH≈5.6时,溶液浓度不变,溶液达到饱和;
D.c(HCO3-)=100%时,溶液的pH=8.
B.由图象可知,A点c(HCO3-)=c(CO32-),溶液呈碱性,则c(OH-)>c( H+);
C.pH≈5.6时,溶液浓度不变,溶液达到饱和;
D.c(HCO3-)=100%时,溶液的pH=8.
解答:
解:A.Na2CO3溶液中存在电荷守恒,为c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故A正确;
B.根据图象分析,A点为碳酸钠和碳酸氢钠的混合溶液,且c(HCO3-)=c(CO32-),溶液呈碱性,则c(OH-)>c( H+),盐溶液水解程度较小,所以c(CO32-)>c(OH-),则离子浓度大小顺序是c(HCO3-)=c(CO32-)>c(OH-)>c( H+),故B错误;
C.pH≈5.6时,溶液浓度不变,溶液达到饱和,说明常温下CO2饱和溶液的pH约为5.6,故C正确;
D.c(HCO3-)=100%时,溶液的pH=8,说明0.05mol/L NaHCO3溶液的pH=8,当加入20 mL盐酸时Na2CO3溶液和盐酸反应生成碳酸氢钠溶液,故D正确.
故选B.
B.根据图象分析,A点为碳酸钠和碳酸氢钠的混合溶液,且c(HCO3-)=c(CO32-),溶液呈碱性,则c(OH-)>c( H+),盐溶液水解程度较小,所以c(CO32-)>c(OH-),则离子浓度大小顺序是c(HCO3-)=c(CO32-)>c(OH-)>c( H+),故B错误;
C.pH≈5.6时,溶液浓度不变,溶液达到饱和,说明常温下CO2饱和溶液的pH约为5.6,故C正确;
D.c(HCO3-)=100%时,溶液的pH=8,说明0.05mol/L NaHCO3溶液的pH=8,当加入20 mL盐酸时Na2CO3溶液和盐酸反应生成碳酸氢钠溶液,故D正确.
故选B.
点评:本题考查了离子浓度大小的比较,为高频考点,侧重于学生的分析能力的考查,注意根据物料守恒、电荷守恒来分析解答,难点是B,注意把握图象曲线的变化特点,难度中等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
有4种混合溶液,分别由等体积0.1mol?L-1的2种溶液混合而成:①CH3COONa与NaCl;②CH3COONa与NaOH;③CH3COONa与NaHSO4;④CH3COONa与NaHCO3,c(CH3COO-)排序正确的是( )
| A、②>④>③>① |
| B、②>④>①>③ |
| C、③>①>②>④ |
| D、①>④>③>② |
在一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g).2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol?L-1.下列判断错误的是( )
| A、平衡常数约为0.3 |
| B、B的转化率为40% |
| C、A的平均反应速率为0.3 mol?(L?min)-1 |
| D、若混合气体的相对分子质量不变则表明该反应达到平衡状态 |
在一定的温度下,浓度都是3mol/L的两种气体A2和B2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别是c(A2)=1.2mol/L,c(B2)=2.4mol/L,c(Z)=1.2mol/L.则该反应的反应式可以表示为( )
| A、A2+2B2=2AB2 |
| B、2A2+B2=2A2B |
| C、3A2+B2=2A3B |
| D、A2+3B2=2AB3 |
下列家庭化学小实验不能达到预期目的是( )
| A、用米汤检验食用加碘盐中含有碘 |
| B、用醋、石灰水验证蛋壳中含有碳酸盐 |
| C、用碘酒检验葡萄中是否含有淀粉 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z最外层电子数相同,Z的核电荷数是W的2倍.元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是( )
| A、原子半径的大小顺序:rY>rX>rQ>rW |
| B、X、Y的最高价氧化物的水化物之间不能发生反应 |
| C、Z元素的氢化物稳定性大于W元素的氢化物稳定性 |
| D、元素Q和Z能形成QZ2型的共价化合物 |