题目内容
5.某学习小组研究铜片和酸反应的情况:(1)在热水浴中进行3个实验,部分实验报告如下表所示
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 在稀硫酸中加铜片 | 无明显变化 |
| Ⅱ | 在硝酸钠溶液中加入铜片 | 无明显变化 |
| Ⅲ | 在稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入铜片 | 有无色气泡;溶液变蓝色 |
②实验Ⅲ中反应的本质是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(用离子方程式表示).
(2)甲同学提出:改变反应条件,可以实现金属铜和稀硫酸反应.
①将铜片放入盛有稀硫酸的烧杯中,不断向稀硫酸中加入过氧化氢并加热烧杯,发现铜片开始溶解,溶液逐渐变蓝色,过氧化氢在该实验中的作用是作氧化剂,将铜氧化为铜离子.
②利用电化学原理实现铜溶于稀硫酸并放出氢气.请画出简易装置图(标明电极,电解质溶液成分).
分析 (1)①实验Ⅰ是证明铜不与稀硫酸反应,实验Ⅱ是验证铜和硝酸根离子不能反应;
②稀硫酸中加入硝酸钠溶液中,形成了稀硝酸,再加入铜片被稀硝酸氧化生成硝酸铜、一氧化氮和水;
(2)①过氧化氢具有氧化性,将铜氧化成了铜离子;
②铜与稀硫酸不反应是非自发的反应,需要设计成电解池发生,铜溶于稀硫酸并生成氢气,铜做阳极,稀硫酸做电解质溶液,阴极可为石墨.
解答 解:(1)①实验Ⅰ是证明铜不与稀硫酸反应,实验Ⅱ是验证铜和硝酸根离子不能反应,
故答案为:证明Cu不与H+、NO3-单独反应;
②稀硫酸中加入硝酸钠溶液中,形成了稀硝酸,再加入铜片被稀硝酸氧化生成硝酸铜、一氧化氮和水,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(2)①将铜片放入盛有稀硫酸的烧杯中,不断向稀硫酸中加入过氧化氢并加热烧杯,发现铜片开始溶解,溶液逐渐变蓝色,过氧化氢具有氧化性,将铜氧化成了铜离子;
故答案为:作氧化剂,将铜氧化为铜离子;
②铜与稀硫酸不反应是非自发的反应,需要设计成电解池发生,铜溶于稀硫酸并生成氢气,铜做阳极,稀硫酸做电解质溶液,阴极可为碳(石墨),装置图为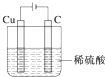 ,
,
故答案为: .
.
点评 本题考查了稀硝酸的性质应用,电解原理的应用,电解原理的理解是解题关键,题目难度中等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
15.下列反应的离子方程式正确的是( )
| A. | 大理石与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 在氯化铝溶液中滴加过量的氨水:Al3++4 OH-═[Al (OH)4]- | |
| C. | 在氢氧化钠溶液中通入过量的CO2:2OH-+CO2═CO32-+H2O | |
| D. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-═SiO32-+H2O |
16.下列物质中,属于共价化合物的是( )
| A. | MgCl2 | B. | HCl | C. | NH4Cl | D. | Na2O2 |
20.酯X与奎宁酸(结构简述如图)互为同分异构体,酯X水解得到2molHCOOH和1mol醇Y,醇Y的分子式为( )

| A. | C4H10O3 | B. | C5H12O4 | C. | C4H12O4 | D. | C5H12O5 |
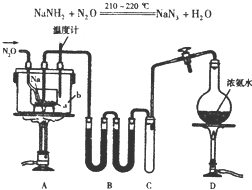 NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:
NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下: