题目内容
4.铁及其化合物在国民经济、日常生活中占有非常重要的地位,了解铁及其化合物的性质和用途非常重要.请回答下列问题:(1)铁在自然界中以化合态存在,其氧化物呈黑色的是FeO、Fe3O4,呈红棕色的是Fe2O3(填写化学式).
(2)铁在纯氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(3)铁合金有下列数据:
| 钢 | |||
| 碳素钢(Fe、C、Mn、Si) | 合金钢 | ||
| 低碳钢 | 中碳钢 | 高碳钢 | 碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% | 含碳量0.3%~0.6% | 含碳量>0.6% | |
| 韧性好,强度低 | 韧性好、强度好 | 硬而脆 | 具有特殊性能 |
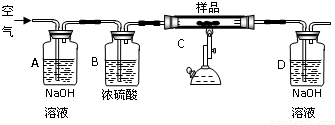
①A、B的作用是除去空气中的二氧化碳和水蒸气,
②充分加热完全反应后,D装置质量增加0.33g,该样品属于中碳钢.
③没有A、B装置,实验结果偏高(填“偏高”“偏低”“不影响”)
分析 (1)根据铁的活泼性和其氧化物的性质来判断;
(2)磁性氧化铁是四氧化三铁,生成四氧化三铁的反应有铁在氧气中点燃和铁在水蒸气下高温反应制得;
(3)①根据实验目的回答;
②根据实验原理,D装置质量增加0.33g即生成的二氧化碳的质量,再根据碳守恒计算;
③没有AB,则二氧化碳变大,则含碳量变大.
解答 解:(1)根据铁在空气中易被氧化,故铁是以化合态存在;其氧化物呈黑色的是FeO、Fe3O4,氧化物中颜色是红色的是Fe2O3,故答案为:化合;FeO、Fe3O4;Fe2O3;
(2)磁性氧化铁是四氧化三铁,生成四氧化三铁的反应有3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(3)①根据实验原理分析,进入样品的空气不能含二氧化碳和水蒸气,所以AB的作用就是除去空气中的二氧化碳和水蒸气,故答案为:除去空气中的二氧化碳和水蒸气;
②根据实验原理,D装置质量增加0.33g即生成的二氧化碳的质量,再根据碳守恒则样品中的碳的质量为:$\frac{033}{44}$×12=0.09g,碳的质量分数为$\frac{0.09}{25}$×100%=0.36%
所以为中碳钢,故答案为:中碳;
③没有AB,则二氧化碳偏大,则含碳量偏高,故答案为:偏高.
点评 本题考查无机物推断,属于开放性题目,需要学生熟练掌握元素化合物知识,中计算关键清楚个阶段发生的反应,注意利用守恒思想解答,难度中等.

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 | |
| C. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| D. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
| A. | 乙醇和乙酸分子都能和金属钠反应 | |
| B. | 乙酸能溶于水,但不溶于乙醇 | |
| C. | 乙醇和乙酸均能使紫色石蕊试液变红 | |
| D. | 乙醇和乙酸互为同分异构体 |
| A. | NaHCO3═CO32-+H++Na+ | B. | S2-+H2O?H2S+2 OH- | ||
| C. | H3PO4?3H++PO43- | D. | NH3•H2O?NH4++OH- |
| A. | ①戊烷②丙烷③丁烷沸点高低顺序为①>③>② | |
| B. | CH4与Cl2以体积比1:4混合,光照时可制得纯净的CCl4 | |
| C. | 苯能在一定条件下跟H2加成生成环己烷 | |
| D. | CH2=CH2+H2O→CH3-CH2OH 是加成反应 |
| A. | 向氯化钙溶液中通入CO2:Ca2++H2O+CO2═CaCO3↓+2H+ | |
| B. | 稀硫酸与氧化铜反应:O2-+2H+═H2O | |
| C. | 碳酸钡与盐酸反应:BaCO3+2H+═Ba2++CO2↑+H2O | |
| D. | 将氯气通入碱溶液中:Cl2+OH-═Cl-+ClO-+H2O |
Ksp(CaCO3)=2.8×10-9、Ksp(MgCO3)=6.8×10-6,
Ksp[Mg(OH)2]=1.8×10-11.
| 海水成分 | Na+ | Ca2+ | Mg2+ | HCO3- | Zn2+ |
| 含量/mol•L-1 | 0.4 | 0.002 | 0.045 | 0.002 | 10-7 |
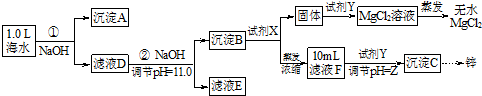
[假设①②过程溶液体积不变,忽略分离过程的损失]
(1)25℃时测得海水的pH> 7.0(填“>”、“<”、“﹦”),其原因是(写离子方程式)HCO3-+H2O?H2CO3+OH-.
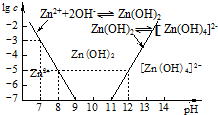
(2)如图为溶液pH与对应的Zn2+、[Zn(OH)4]2-物质的量浓度的对数坐标图.请结合图中数据回答:试剂Y的化学式为HCl;由滤液F到沉淀C过程(一般认为离子浓度低于10-5mol/L就是沉淀完全),则调节的pH范围为8<pH<12.
(3)同学们发现,把MgCl2溶液蒸干、灼烧所得的白色固体难溶于水,你认为其主要成分是MgO.原因是(用化学方程式表示)MgCl2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2HCl↑、Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
(4)由图中c(Zn2+)计算Zn(OH)2的溶度积Ksp=10-17.