题目内容
14.下列叙述错误的是( )| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 | |
| C. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| D. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
分析 A.苯与溴水不反应;
B.淀粉水解生成葡萄糖,油脂水解生成高级脂肪酸和甘油,蛋白质水解生成氨基酸;
C.乙酸具有酸性,油脂可在碱性条件下水解;
D.乙酸与碳酸钠反应.
解答 解:A.乙烯含有碳碳双键和单质溴发生加成反应,苯和溴水发生的是萃取,故A错误;
B.淀粉为多糖,水解生成葡萄糖,油脂水解生成高级脂肪酸和甘油,蛋白质水解生成氨基酸,故B正确;
C.乙酸具有酸性,油脂含有酯基,可在碱性条件下水解,故C正确;
D.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应,故D正确.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握物质的性质、有机反应、有机物组成等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
4.下列仪器:①天平;②容量瓶;③蒸馏烧瓶;④漏斗;⑤分液漏斗;⑥试管,用于分离物质的是( )
| A. | ①③④ | B. | ①②⑥ | C. | ③④⑤ | D. | ③④⑥ |
2.Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的是( )(已知Na2O与水反应生成NaOH)
①钠的化合物②能与硝酸反应的物质 ③可溶于水的物质 ④水溶液导电 ⑤钠盐 ⑥钠的含氧化合物.
①钠的化合物②能与硝酸反应的物质 ③可溶于水的物质 ④水溶液导电 ⑤钠盐 ⑥钠的含氧化合物.
| A. | ①④⑤ | B. | ①②⑤⑥ | C. | ①③④ | D. | ②⑤⑥ |
9.下列设计的实验方案能达到实验目的是( )
| A. | 检验淀粉是否完全水解:取少量水解液于试管中,加入过量氢氧化钠溶液和新制Cu(OH)2悬浊液,加热至沸腾,看是否有砖红色沉淀生成 | |
| B. | 提纯混有少量CaCl2的NaCl固体:将固体配成溶液,加入稍过量Na2CO3溶液至沉淀完全,过滤,再向滤液中加入稍过量盐酸,蒸发结晶 | |
| C. | 制取少量乙酸乙酯:向试管中加入浓硫酸,再加入无水乙醇,冷却后加入冰醋酸,加热,将生成的蒸气导至盛有氢氧化钠溶液的试管中 | |
| D. | 验证炭与浓硫酸反应产生的CO2:将炭与浓硫酸反应生成的气体通入盛有澄清石灰水的试管中,观察是否有白色沉淀生成 |
19.乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为:
2CO(g)+4H2(g)?CH3CH2OH(g)+H2O(g)△H=-256.1kJ•mol-1
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1
(1)以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=-173.7kJ•mol-1.
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.
①某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图1.若不使用CO,温度超过800℃,发现NO的转化率降低,其可能的原因为该反应是放热反应,升高温度反应更有利于向逆反应方向进行;在n(NO)/n(C O)=1的条件下,应控制的最佳温度在900℃左右.
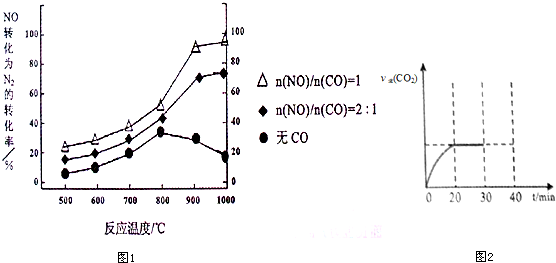
②用活性炭还原法处理氮氧化物.有关反应为:C (s)+2NO2(g)?N2 (g)+CO2 (g).某研究小组向某密闭容器中加人足量的活性炭和NO,恒温( T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
I.根据表中数据,求反应开始至20min以v(NO)表示的反应速率为0.030mol•L-1•mol-1(保留两位有效数字),T1℃时该反应的平衡常数为0.56(保留两位有效数字).
II.30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减小CO2的浓度.图2表示CO2的逆反应速率[v逆(CO2)]随反应时间的变化关系图.请在图中画出在30min改变上述条件时,在40min时刻再次达到平衡的变化曲线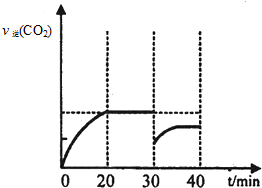 .
.
2CO(g)+4H2(g)?CH3CH2OH(g)+H2O(g)△H=-256.1kJ•mol-1
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1
(1)以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=-173.7kJ•mol-1.
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.
①某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图1.若不使用CO,温度超过800℃,发现NO的转化率降低,其可能的原因为该反应是放热反应,升高温度反应更有利于向逆反应方向进行;在n(NO)/n(C O)=1的条件下,应控制的最佳温度在900℃左右.

②用活性炭还原法处理氮氧化物.有关反应为:C (s)+2NO2(g)?N2 (g)+CO2 (g).某研究小组向某密闭容器中加人足量的活性炭和NO,恒温( T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度/mol?L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
II.30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减小CO2的浓度.图2表示CO2的逆反应速率[v逆(CO2)]随反应时间的变化关系图.请在图中画出在30min改变上述条件时,在40min时刻再次达到平衡的变化曲线
 .
.
6.在实验室里可用如图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质.
图中:
①为氯气发生装置;
②的试管里盛有15mL30%NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
请填写下列空白:
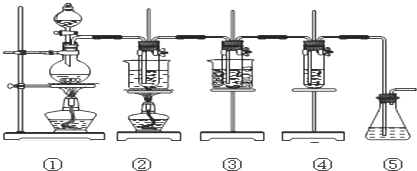
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有C(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气小于0.06mol.(填“大于”“小于”或“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的物质的量为0.4mol.
(3)写出装置②中发生反应的化学方程式3Cl2+6NaOH$\frac{\underline{\;\;△\;\;}}{\;}$5NaCl+NaClO3+3H2O.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
图中:
①为氯气发生装置;
②的试管里盛有15mL30%NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
请填写下列空白:

(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有C(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气小于0.06mol.(填“大于”“小于”或“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的物质的量为0.4mol.
(3)写出装置②中发生反应的化学方程式3Cl2+6NaOH$\frac{\underline{\;\;△\;\;}}{\;}$5NaCl+NaClO3+3H2O.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | HClO有强氧化性,体现漂白作用是其褪色 |
| 然后溶液从无色逐渐变为浅绿色 | 溶液中溶解了大量的氯气,体现浅绿色 |
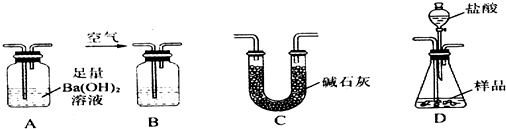
4.铁及其化合物在国民经济、日常生活中占有非常重要的地位,了解铁及其化合物的性质和用途非常重要.请回答下列问题:
(1)铁在自然界中以化合态存在,其氧化物呈黑色的是FeO、Fe3O4,呈红棕色的是Fe2O3(填写化学式).
(2)铁在纯氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(3)铁合金有下列数据:
取25g某碳素钢样品,按下列实验流程进行操作:
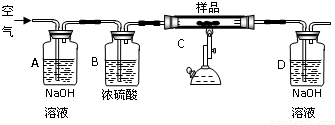
①A、B的作用是除去空气中的二氧化碳和水蒸气,
②充分加热完全反应后,D装置质量增加0.33g,该样品属于中碳钢.
③没有A、B装置,实验结果偏高(填“偏高”“偏低”“不影响”)
(1)铁在自然界中以化合态存在,其氧化物呈黑色的是FeO、Fe3O4,呈红棕色的是Fe2O3(填写化学式).
(2)铁在纯氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(3)铁合金有下列数据:
| 钢 | |||
| 碳素钢(Fe、C、Mn、Si) | 合金钢 | ||
| 低碳钢 | 中碳钢 | 高碳钢 | 碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% | 含碳量0.3%~0.6% | 含碳量>0.6% | |
| 韧性好,强度低 | 韧性好、强度好 | 硬而脆 | 具有特殊性能 |

①A、B的作用是除去空气中的二氧化碳和水蒸气,
②充分加热完全反应后,D装置质量增加0.33g,该样品属于中碳钢.
③没有A、B装置,实验结果偏高(填“偏高”“偏低”“不影响”)