题目内容
15.下列关于乙醇和乙酸的说法中,正确的是( )| A. | 乙醇和乙酸分子都能和金属钠反应 | |
| B. | 乙酸能溶于水,但不溶于乙醇 | |
| C. | 乙醇和乙酸均能使紫色石蕊试液变红 | |
| D. | 乙醇和乙酸互为同分异构体 |
分析 乙醇中含-OH,乙酸中含-COOH,均与Na反应,均与水形成氢键,二者分子式不同,且乙醇为中性,以此来解答.
解答 解:A.乙醇和乙酸分子都能和金属钠反应生成氢气,故A正确;
B.乙酸能溶于水,且溶于乙醇,故B错误;
C.乙酸能使紫色石蕊试液变红,乙醇不能,故C错误;
D.乙醇和乙酸分子式不同,不互为同分异构体,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质、有机反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
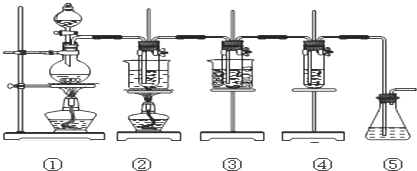
6.在实验室里可用如图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质.
图中:
①为氯气发生装置;
②的试管里盛有15mL30%NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有C(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气小于0.06mol.(填“大于”“小于”或“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的物质的量为0.4mol.
(3)写出装置②中发生反应的化学方程式3Cl2+6NaOH$\frac{\underline{\;\;△\;\;}}{\;}$5NaCl+NaClO3+3H2O.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
图中:
①为氯气发生装置;
②的试管里盛有15mL30%NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
请填写下列空白:

(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有C(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气小于0.06mol.(填“大于”“小于”或“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的物质的量为0.4mol.
(3)写出装置②中发生反应的化学方程式3Cl2+6NaOH$\frac{\underline{\;\;△\;\;}}{\;}$5NaCl+NaClO3+3H2O.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | HClO有强氧化性,体现漂白作用是其褪色 |
| 然后溶液从无色逐渐变为浅绿色 | 溶液中溶解了大量的氯气,体现浅绿色 |
10.下列离子方程式中,正确的是( )
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 硫酸钠溶液与氯化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| C. | 盐酸滴在石灰石上:CaCO3+2H+═H2CO3+Ca2+ | |
| D. | 氧化铜与硫酸混合:Cu2++SO42-═CuSO4 |
20.称取铁粉和氧化铜的混合物6.40g,进行如下实验:
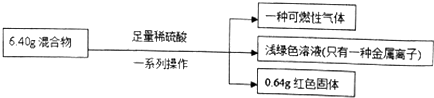
根据实验所得数据,下列说法不正确的是( )

根据实验所得数据,下列说法不正确的是( )
| A. | 原混合物中铜元素的质量一定为0.64g | |
| B. | 生成气体体积为2.016L | |
| C. | 实验中反应的硫酸的物质的量为0.1mol | |
| D. | 原混合物中铁的质量分数为87.5% |
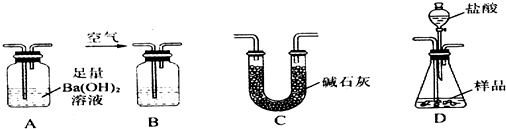
4.铁及其化合物在国民经济、日常生活中占有非常重要的地位,了解铁及其化合物的性质和用途非常重要.请回答下列问题:
(1)铁在自然界中以化合态存在,其氧化物呈黑色的是FeO、Fe3O4,呈红棕色的是Fe2O3(填写化学式).
(2)铁在纯氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(3)铁合金有下列数据:
取25g某碳素钢样品,按下列实验流程进行操作:
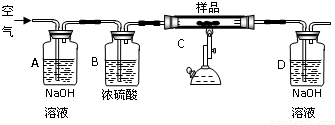
①A、B的作用是除去空气中的二氧化碳和水蒸气,
②充分加热完全反应后,D装置质量增加0.33g,该样品属于中碳钢.
③没有A、B装置,实验结果偏高(填“偏高”“偏低”“不影响”)
(1)铁在自然界中以化合态存在,其氧化物呈黑色的是FeO、Fe3O4,呈红棕色的是Fe2O3(填写化学式).
(2)铁在纯氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(3)铁合金有下列数据:
| 钢 | |||
| 碳素钢(Fe、C、Mn、Si) | 合金钢 | ||
| 低碳钢 | 中碳钢 | 高碳钢 | 碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% | 含碳量0.3%~0.6% | 含碳量>0.6% | |
| 韧性好,强度低 | 韧性好、强度好 | 硬而脆 | 具有特殊性能 |

①A、B的作用是除去空气中的二氧化碳和水蒸气,
②充分加热完全反应后,D装置质量增加0.33g,该样品属于中碳钢.
③没有A、B装置,实验结果偏高(填“偏高”“偏低”“不影响”)
5.下列实验的现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| A. | A | B. | B | C. | C | D. | D |