题目内容
2.下列叙述中正确的是( )| A. | 体积相同、浓度均为0.1 mol•L-1的NaOH溶液、氨水,分别稀释m倍、n倍,溶液的pH都变成9,则m<n | |
| B. | 有甲、乙两氨水溶液,测得甲的pH=a,乙的pH=a+1,则甲乙两溶液c(H+)之比为10:1 | |
| C. | 相同温度下,0.2 mol•L-1乙酸溶液与0.1 mol•L-1乙酸溶液中c(H+)之比为2:1 | |
| D. | 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,K=$\frac{c{α}^{2}}{c(1-α)}$.若加入少量醋酸钠固体,则CH3COOH?CH3COO-+H+向左移动,α减小,K变小 |
分析 A、氢氧化钠是强电解质,一水合氨是弱电解质,相同浓度的两种溶液中,氢氧化钠溶液的pH大于氨水,加水稀释促进一水合氨电离,但一水合氨仍然存在电离平衡;
B、c(H+)=10-pH;
C、醋酸是弱酸,越稀越电离;
D、弱电解质的电离平衡常数只与温度有关.
解答 解:A、氢氧化钠是强电解质完全电离,一水合氨是弱电解质,在水溶液里部分电离,相同浓度的两种溶液中,氢氧化钠溶液的pH大于氨水,加水稀释促进一水合氨电离,但一水合氨仍然存在电离平衡,电离程度仍然小于氢氧化钠,所以要使稀释后溶液的PH相等,则氢氧化钠需要稀释倍数大于氨水,即m>n,故A错误;
B、c(H+)=10-pH,故pH=a的氨水溶液中氢离子浓度为10-amol/L,pH=a+1的乙酸溶液中的氢离子浓度为10-(a+1)mol/L,故甲乙两溶液c(H+)之比为10:1,故B正确;
C、醋酸是弱酸,越稀越电离,故0.2 mol•L-1乙酸溶液的电离程度小于0.1 mol•L-1乙酸溶液的电离程度,故c(H+)之比小于2:1,故C错误;
D、弱电解质的电离平衡常数只与温度有关,温度不变是,醋酸的电离平衡常数不变,但稀释醋酸溶液时促进醋酸电离,导致醋酸的电离度增大,故D错误.
故选B.
点评 本题考查了弱电解质的电离、影响弱电解质电离的因素等知识点,明确弱电解质电离特点是解本题关键,注意电离平衡常数、水解平衡常数、化学平衡常数、溶度积常数等都只与温度有关,与溶液的酸碱性无关,为易错点.

练习册系列答案
相关题目
18.在一定温度下,对可逆反应A(g)+3B(g)?4C(g)的下列叙述中,能说明反应已经达到达到平衡的是( )
| A. | C的生成速率与C的分解速率相等 | |
| B. | 单位时间内amol A生成,同时生成3amol B | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体的平均相对分子质量不变 |
10.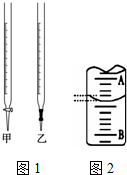 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①取一支图1所示仪器,用蒸馏水洗净,即加入待测的NaOH溶液,
使尖嘴部分充满溶液,并调整液面处于“0“刻度以下的位置,记下读数;
②取锥形瓶用蒸馏水洗净,精确量取一定量的0.1000mol•L-1标准盐酸;
③加入3滴酚酞试液,摇匀;
④进行滴定实验,并记录数据.
⑤重复以上步骤2次.
回答下列问题:
(1)步骤①中应将NaOH溶液注入图中的碱式滴定管(填仪器名称)中.
(2)在步骤①中存在的明显错误是滴定管没有用待测NaOH溶液润洗,由此会使测定结果偏低(选填“偏高”、“偏低”或“无影响”).
(3)图2是某次实验中液面位置示意图,若A与B刻度间相差1mL,A处的刻度为19,滴定管中液面读数应为19.40mL.
(4)操作④中左手轻轻挤压玻璃球,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,能确定实验终点的现象是加入最后一滴液体,溶液由无色变成浅红色,且半分钟内不褪色.
(5)根据下列数据:
计算待测烧碱溶液的浓度为0.1053 mol/L(保留至小数点后四位).
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①取一支图1所示仪器,用蒸馏水洗净,即加入待测的NaOH溶液,
使尖嘴部分充满溶液,并调整液面处于“0“刻度以下的位置,记下读数;
②取锥形瓶用蒸馏水洗净,精确量取一定量的0.1000mol•L-1标准盐酸;
③加入3滴酚酞试液,摇匀;
④进行滴定实验,并记录数据.
⑤重复以上步骤2次.
回答下列问题:
(1)步骤①中应将NaOH溶液注入图中的碱式滴定管(填仪器名称)中.
(2)在步骤①中存在的明显错误是滴定管没有用待测NaOH溶液润洗,由此会使测定结果偏低(选填“偏高”、“偏低”或“无影响”).
(3)图2是某次实验中液面位置示意图,若A与B刻度间相差1mL,A处的刻度为19,滴定管中液面读数应为19.40mL.
(4)操作④中左手轻轻挤压玻璃球,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,能确定实验终点的现象是加入最后一滴液体,溶液由无色变成浅红色,且半分钟内不褪色.
(5)根据下列数据:
| 滴定次数 | 标准盐酸体积/mL | 待测液体积/mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.52 | 19.42 |
| 第二次 | 20.00 | 4.07 | 23.17 |
| 第三次 | 20.00 | 1.08 | 20.08 |
17.通过以下反应均可获取H2.下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
| A. | 反应①中电能转化为化学能 | |
| B. | 反应②为放热反应 | |
| C. | 反应③使用催化剂,△H3减小 | |
| D. | 反应CH4(g)=C(s)+2H2(g)的△H=+74.8 kJ•mol-1 |