题目内容
7.下列陈述Ⅰ和Ⅱ均正确,并存在因果关系的是( )| 陈述Ⅰ | 陈述Ⅱ | |
| A | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| B | 非金属性:Cl>S | 酸性:HClO3>H2SO4 |
| C | 常温下,NaHCO3的溶解度比Na2CO3小 | 向饱和Na2CO3溶液中通入CO2产生沉淀 |
| D | 常温下,SO2与氢硫酸和NaOH溶液均可反应 | SO2是两性氧化物 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.CaCl2与空气中的CO2不反应;
B.HClO3不是最高价含氧酸;
C.向饱和Na2CO3溶液中通入CO2产生沉淀,析出碳酸氢钠,可比较溶解度大小;
D.SO2是酸性氧化物.
解答 解:A.CaCl2与空气中的CO2不反应,漂白粉在空气中久置变质,因次氯酸钙与水、二氧化碳反应,故A错误;
B.HClO3不是最高价含氧酸,由非金属性:Cl>S,可知酸性:HClO4>H2SO4,故B错误;
C.向饱和Na2CO3溶液中通入CO2产生沉淀,析出碳酸氢钠,则常温下,NaHCO3的溶解度比Na2CO3小,故C正确;
D.SO2是酸性氧化物,SO2与氢硫酸和NaOH溶液分别发生氧化还原反应、复分解反应,故D错误;
故选C.
点评 本题考查物质的性质及反应,为高频考点,把握发生的反应、非金属性比较等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
1.下列有关物质的性质或应用的说法正确的是( )
| A. | 用核磁共振氢谱鉴别1-丙醇和2-丙醇 | |
| B. | 用酸性KMnO4溶液除去乙烷中混有的乙烯 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
2.请回答下列问题:
(1)纯水在T℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=10-12 mol•L-1.
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等.若将两溶液稀释相同的倍数后,pH(A)<pH(B) (填“>”、“=”或“<”).现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)<V(B)(填“>”、“=”或“<”).
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR-,HR-?R2-+H+,若0.1mol•L-1NaHR溶液的c(H+)=a mol•L-1,则0.1mol•L-1H2R溶液中c(H+)< (0.1+a) mol•L-1(填“<”、“>”或“=”),理由是H2R中第一步电离出的H+对HR-的电离产生了抑制作用.
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
①25℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为H2CO3>HCN>CH3COOH(用化学式表示).
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(1)纯水在T℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=10-12 mol•L-1.
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等.若将两溶液稀释相同的倍数后,pH(A)<pH(B) (填“>”、“=”或“<”).现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)<V(B)(填“>”、“=”或“<”).
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR-,HR-?R2-+H+,若0.1mol•L-1NaHR溶液的c(H+)=a mol•L-1,则0.1mol•L-1H2R溶液中c(H+)< (0.1+a) mol•L-1(填“<”、“>”或“=”),理由是H2R中第一步电离出的H+对HR-的电离产生了抑制作用.
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
15.下列离子方程式正确的是( )
| A. | 氧化铁和盐酸:O2-+2H+═H2O | |
| B. | 向澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| C. | 澄清石灰水和Ca(HCO3)2溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氢氧化钡溶液和硫酸镁溶液反应:Ba2++SO42-═BaSO4↓ |
2.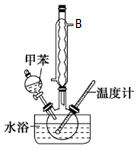 硝基甲苯有领、间、对三种,其中对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备.一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h.反应结束后,过滤,滤液分别用5%NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯.
硝基甲苯有领、间、对三种,其中对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备.一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h.反应结束后,过滤,滤液分别用5%NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯.
请回答下列问题:
(1)仪器B的名称是球形冷凝管,其作用是冷凝、回流.
(2)过滤在分液漏斗中洗涤静后,有机层处于下层(填“上”或“下”)放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有分液漏斗上口塞子未打开.
(3)上述新的试验方法中过滤的目的是回收NaHSO4,滤液用5%NaHCO3溶液洗涤的原因是除去硫酸、硝酸、乙酸.
(4)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果.
催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为0.32,此时若使用13.0g甲苯,分离出对硝基甲苯的质量是8.8g(保留一位小数).
②由表中数据可知甲苯硝化主要得到对硝基甲苯和邻硝基甲苯,原因是苯环上的甲基使苯环上连接甲基的碳原子的邻对位硝化反应更容易进行.
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优有在硝化产物中对硝基甲苯比例提高(或催化剂用量少且能循环使用)(回答一条)
④对硝基甲苯和邻硝基甲苯的部分物理特性如表:

其中,操作1的名称为分液;操作2中需要使用下列仪器中的ABC(填序号).
A.冷凝管 B.酒精灯 C.温度计 D.分液漏斗 E.蒸发皿.
 硝基甲苯有领、间、对三种,其中对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备.一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h.反应结束后,过滤,滤液分别用5%NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯.
硝基甲苯有领、间、对三种,其中对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备.一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h.反应结束后,过滤,滤液分别用5%NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯.请回答下列问题:
(1)仪器B的名称是球形冷凝管,其作用是冷凝、回流.
(2)过滤在分液漏斗中洗涤静后,有机层处于下层(填“上”或“下”)放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有分液漏斗上口塞子未打开.
(3)上述新的试验方法中过滤的目的是回收NaHSO4,滤液用5%NaHCO3溶液洗涤的原因是除去硫酸、硝酸、乙酸.
(4)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果.
| 催化剂 | n(催化剂) | 硝化产物中各种异构体质量分数(%) | 总产率 (%) | ||
| n(甲苯) | 对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | ||
| 浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 82.0 |
| 1.2 | 36.5 | 59.2 | 4.0 | 83.8 | |
NaHSO4 | 0.25 | 46.3 | 52.8 | 0.9 | 92.8 |
| 0.32 | 48.0 | 51.7 | 0.3 | 95.0 | |
| 0.36 | 45.0 | 54.4 | 0.6 | 93.9 | |
②由表中数据可知甲苯硝化主要得到对硝基甲苯和邻硝基甲苯,原因是苯环上的甲基使苯环上连接甲基的碳原子的邻对位硝化反应更容易进行.
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优有在硝化产物中对硝基甲苯比例提高(或催化剂用量少且能循环使用)(回答一条)
④对硝基甲苯和邻硝基甲苯的部分物理特性如表:
| 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |

其中,操作1的名称为分液;操作2中需要使用下列仪器中的ABC(填序号).
A.冷凝管 B.酒精灯 C.温度计 D.分液漏斗 E.蒸发皿.
16.用胆矾配制0.2mol/L的CuSO4溶液,下列操作正确的是( )
| A. | 取50g胆矾溶于1L水中 | B. | 取50g胆矾溶于水配成1L溶液 | ||
| C. | 取32g胆矾溶于水配成1L溶液 | D. | 取无水硫酸铜32g溶于1L水中 |