题目内容
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 1L 1mo/L的FeCl3溶液中含有的Fe3+为1NA | |
| B. | 标准状况下,22.4L空气含有NA个单质分子 | |
| C. | 1mol铜与足量硫反应,转移的电子总数为NA | |
| D. | 18g D2O(重水)中所含电子个数为10 NA |
分析 A、铁离子为弱碱阳离子,在溶液中会水解;
B、空气中不全是单质;
C、铜和硫反应后变为+1价;
D、求出重水的物质的量,然后根据重水中含10个电子来分析.
解答 解:A、铁离子为弱碱阳离子,在溶液中会水解,故溶液中的铁离子的个数小于NA个,故A错误;
B、空气中不全是单质,还有化合物,故标况下22.4L空气即1mol空气中含有的单质分子小于NA个,故B错误;
C、铜和硫反应后变为+1价,故1mol反应后转移NA个电子,故C正确;
D、重水的摩尔质量为20g/mol,故18g重水的物质的量为0.9mol,而重水中含10个电子,故0.9mol重水中含9NA个电子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.聚甲基丙烯酸酯( )的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )
)的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )
 )的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )
)的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )| A. | 聚甲基丙烯酸甲酯属于有机高分子合成材料 | |
| B. | 聚甲基丙烯酸甲酯的分子式可表示为(C5H8O2)n | |
| C. | 合成PMMA的单体是甲基丙烯酸和甲醇 | |
| D. | 甲基丙烯酸甲酯中碳原子可能都处于同一平面 |
19.有八种物质:①甲烷、②苯、③聚1,3-丁二烯、④丙烯、⑤2-丁炔、⑥环戊烷、⑦聚乙烯、⑧环己烯,即能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
3.下列说法正确的是( )
| A. | 计算机、光缆在信息产业中有广泛应用,制造光缆和计算机芯片的主要材料都是硅 | |
| B. | 蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 | |
| C. | Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 | |
| D. | 日常生活中无水乙醇常用于杀菌消毒 |
13.下列表示物质结构的化学用语或模型图正确的是( )
| A. | HClO的结构式:H-O-Cl | B. | H2O2的电子式: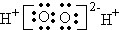 | ||
| C. | 质量数为14碳原子表示方法:14C | D. | 14C的原子结构示意图: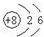 |
20.下列说法正确的是( )
| A. | 体积相等pH=12的氨水和NaOH溶液中和盐酸的能力相同 | |
| B. | 室温下,向NH4HSO4溶液中加入NaOH溶液至中性,则c(SO42-)>c(Na+)>c(NH4+) | |
| C. | 物质的量浓度之比为1:2的CH3COOH和CH3COONa的混合溶液中:2c(CH3COO-)+2c(CH3COOH)=3c(Na+) | |
| D. | 向10ml 0.01mol/L AgNO3溶液中依次滴入2~3滴0.01mol/L NaCl溶液、0.01mol/L NaI溶液,所得沉淀由白色变成黄色,则可推知Kap(AgI)<Kap(AgCl) |
18.1985年科学家发现了C60分子,它由60个碳原子构成,形状像足球,又叫足球烯.下列有关C60的描述正确的是( )
| A. | 它是一种复杂的混合物 | B. | 它由60个碳单质构成 | ||
| C. | 它是一种单质 | D. | 它是一种化合物 |