题目内容
7. A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).
A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).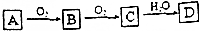
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体.
①D的化学式是H2SO4;
②在工业生产中,B气体的大量排放被雨水吸收后形成了酸雨而污染了环境.
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为过氧化钠,用化学方程式表示该物质与水的反应2Na2O2+2 H2O=4 NaOH+O2↑.将C长期露置于空气中,最后将变成物质D,D的化学式为Na2CO3.现在有D和NaHC03的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为83.2%.
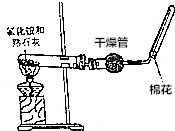
(3)若C是红棕色气体.A是一种能使湿润的红色石蕊试纸变蓝的气体.下图是实验室制取A气体的装置:
①写出实验室制取A的化学方程Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②为了检验氨气是否集满,可将将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满,则证明已收集满.D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
分析 (1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,A与氧气连续反应,则A为S,则B为SO2,C为SO3,D为H2SO4;
(2)若A是一种活泼金属,C是淡黄色固体,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2;
(3)C是红棕色气体,A是一种能使湿润的红色石蕊试纸变蓝的气体,则A为NH3 ,B为NO,C为NO2.
解答 解:(1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,A与氧气连续反应,则A为S,则B为SO2,C为SO3,D为H2SO4,在工业生产中,B气体的大量排放被雨水吸收后形成了酸雨而污染了环境,
故答案为:①H2SO4;②酸雨;
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2,C的名称为过氧化钠,过氧化钠与水的反应:2Na2O2+2 H2O=4 NaOH+O2↑,C长期露置于空气中,过氧化钠与二氧化碳发生反应:2Na2O2+2 CO2=2 Na2CO3+O2↑,过氧化钠与水反应生成氢氧化钠,氢氧化钠也吸收二氧化碳,经过系列变化,最后将变成物质D为Na2CO3,
令混合物中碳酸氢钠的质量为m,则:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O 质量减少
168 62
m 10g-9.38g=0.62g
故m=$\frac{168×0.62g}{62}$=1.68g,故碳酸钠的质量分数=$\frac{10-1.68g}{10g}$×100%=83.2%,
故答案为:过氧化钠; 2Na2O2+2 H2O=4 NaOH+O2↑;Na2CO3;83.2%;
(3)C是红棕色气体,A是一种能使湿润的红色石蕊试纸变蓝的气体,则A为NH3 ,B为NO,C为NO2,
①实验室用氢氧化钙和氯化铵在加热条件下反应准备氨气,反应的方程式为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②检验氨气是否收集满,可将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满,或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满,也可以用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满,
HNO3是强电解质,具有强氧化性,浓硝酸与铜反应的离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,
故答案为:将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满);Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
点评 本题考查无机物推断,是高考中的常见题型,属于基础性试题的考查,试题难易适中,侧重对学生基础知识的巩固训练,物质特殊的颜色是推断的突破口.

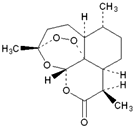 2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )
2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )| A. | 难溶于水,易溶于乙醚 | B. | 在热的NaOH溶液中可发生水解反应 | ||
| C. | 一定条件下能与氯气发生取代反应 | D. | 化学式为C15H21O5 |
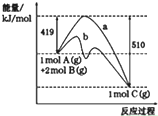
| A. | 曲线b表示使用催化剂后的能量变化 | |
| B. | 正反应活化能大于逆反应活化能 | |
| C. | 由图可知该反应的焓变△H=+91 kJ•mol-1 | |
| D. | 反应中将气体A换为固体反应,其他条件不变,反应放出热量大于91kJ |
| A. | CsOH是一种既可与强酸又可与强碱反应的两性氢氧化物 | |
| B. | Cs在空气中燃烧可生成Cs2O和Cs2O2 | |
| C. | Cs与水反应,能发生爆炸,并放出H2 | |
| D. | CsOH很稳定,加热不易分解 |
| A. | aL气体的平均相对分子质数为41.3 | |
| B. | aL气体被水吸收时转移电子的物质的量为($\frac{2m}{170}-\frac{b}{108}$)mol | |
| C. | cL剩余气体是O2,且c=$\frac{a}{4}$ | |
| D. | 将mgAgNO3溶于水,再加足量的盐酸,$\frac{b}{108}$×143.5g可生成沉淀 |
| A. | 赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 | |
| B. | 为防止寨卡病毒传播,可用漂粉精或双氧水对环境进行消毒 | |
| C. | 大力开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 | |
| D. | 硅酸钠溶液应存放在配有玻璃塞的广口试剂瓶中 |
| A. | 苯酚 | B. | 澄清石灰水 | C. | FeSO4 | D. | Na2SO4 |
| A. | υ正=υ逆≠0时的状态 | B. | NO2全部转变成N2O4的状态 | ||
| C. | c(NO2)=c(N2O4)的状态 | D. | 体系的颜色发生变化的状态 |
 .
.