题目内容
下列电离方程式正确的是( )
| A、NaHCO3═Na++H++CO32- |
| B、Ba(OH)2═Ba2++OH- |
| C、Al2(SO4)3═2Al3++3SO42- |
| D、H2SO4═H2++SO42- |
考点:电离方程式的书写
专题:离子反应专题
分析:A.碳酸为弱酸,碳酸氢钠中的氢离子不能完全电离;
B.电荷不守恒;
C.硫酸铝为强电解质,完全电离,用“=”号,电荷守恒、离子符号正确;
D.氢离子的符号书写错误.
B.电荷不守恒;
C.硫酸铝为强电解质,完全电离,用“=”号,电荷守恒、离子符号正确;
D.氢离子的符号书写错误.
解答:
解:A.碳酸为弱酸,碳酸氢钠中的氢离子不能完全电离,其电离方程式为:NaHCO3═Na++HCO3-,故A错误;
B.氢氧化钡在溶液中完全电离,其电离方程式为:Ba(OH)2═Ba2++2OH-,故B错误;
C.硫酸铝为强电解质,完全电离,用“=”号,电荷守恒、离子符号正确,其电离方程式为:Al2(SO4)3═2Al3++3SO42-,故C正确;
D.氢离子的符号书写错误,硫酸为强电解质,完全电离其电离方程式为:H2SO4═2H++SO42-,故D错误.
故选C.
B.氢氧化钡在溶液中完全电离,其电离方程式为:Ba(OH)2═Ba2++2OH-,故B错误;
C.硫酸铝为强电解质,完全电离,用“=”号,电荷守恒、离子符号正确,其电离方程式为:Al2(SO4)3═2Al3++3SO42-,故C正确;
D.氢离子的符号书写错误,硫酸为强电解质,完全电离其电离方程式为:H2SO4═2H++SO42-,故D错误.
故选C.
点评:本题主要考查电离方程式书写,掌握正确书写电离方程式的方法,并能正确判断电离方程式的正误是解答关键,题目难度不大.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
1mol气态钠离子和1mol气态氯离子结合生成1mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能.下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是( )
| A、Na+(g)+Cl-(g)═NaCl(s)△H |
| B、Na(s)+12Cl2(g)═NaCl(s)△H1 |
| C、Na(g)-e-═Na+(g)△H2 |
| D、Cl(g)+e-═Cl-(g)△H3 |
环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的.下列环境问题与所对应的物质不相关的是( )
| A、温室效应--二氧化碳 |
| B、光化学污染--二氧化氮 |
| C、酸雨--二氧化碳 |
| D、臭氧层破坏--氟氯烃 |
两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法错误的是( )
| A、若a=b=3,8>m>n>b,则元素非金属性:X>Y |
| B、若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y<X |
| C、若Y的气态氢化物化学式为YHn,且b<4,则该氢化物易溶于水 |
| D、若a<b=3,m=n=7,已知原子半径大小:Y>N(氮原子)>X,则NX3、NY3与水反应生成不同的含氮化合物 |
下列离子方程式正确的是( )
| A、将少量石灰水滴入碳酸氢钠溶液中 HCO3-+Ca2++OH-═CaCO3↓+H2O | ||||
B、碳酸氢铵与足量氢氧化钠两种浓溶液混合加热 NH4++OH-
| ||||
| C、用惰性电极电解氯化钠溶液 2H2O+2Cl-═Cl2↑+H2↑+2OH- | ||||
| D、亚硝酸钠水溶液显碱性 NO2-+H2O?HNO2+OH- |
取一定质量含Cu、Cu2O、CuO的固体混合物,将其分成两等份并进行下列转化,
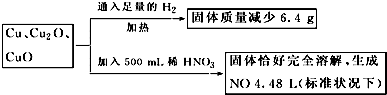
则转化过程中所加稀HNO3的物质的量浓度为( )

则转化过程中所加稀HNO3的物质的量浓度为( )
| A、4.4 mol?L-1 |
| B、3.6 mol?L-1 |
| C、4.0 mol?L-1 |
| D、3.2 mol?L-1 |