题目内容
配平下列化学方程式,并指出其中的还原剂:
H2S+ HNO3(浓)- H2SO4+ NO2↑+ H2O,
还原剂是 .
还原剂是
考点:氧化还原反应方程式的配平
专题:氧化还原反应专题
分析:该反应中S元素化合价由-2价变为+6价,N元素化合价由+5价变为+4价,其转移电子总数为8,再结合原子守恒配平方程式;
解答:
解:该反应中S元素化合价由-2价变为+6价,N元素化合价由+5价变为+4价,得失电子的最小公倍数为8,H2S的系数为1,HNO3的系数为8,根据原子守恒,H2SO4的系数为1,NO2
的系数为8,H2O的系数为4,故反应方程式为H2S+8HNO3(浓)=H2SO4+8NO2↑+4H2O;反应中失电子价态升高的作还原剂,故还原剂是H2S.
故答案为:1;8;1;8;4;H2S.
的系数为8,H2O的系数为4,故反应方程式为H2S+8HNO3(浓)=H2SO4+8NO2↑+4H2O;反应中失电子价态升高的作还原剂,故还原剂是H2S.
故答案为:1;8;1;8;4;H2S.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列电离方程式正确的是( )
| A、NaHCO3═Na++H++CO32- |
| B、Ba(OH)2═Ba2++OH- |
| C、Al2(SO4)3═2Al3++3SO42- |
| D、H2SO4═H2++SO42- |
下列各组物质的无色溶液,不用其他试剂即可鉴别的是( )
①KOH Na2SO4 AlCl3
②NaHCO3 Ba(OH)2 H2SO4
③盐酸 Na[Al(OH)4]NaHSO4
④Ca(OH)2 Na2CO3 BaCl2.
①KOH Na2SO4 AlCl3
②NaHCO3 Ba(OH)2 H2SO4
③盐酸 Na[Al(OH)4]NaHSO4
④Ca(OH)2 Na2CO3 BaCl2.
| A、①② | B、②③ |
| C、①③④ | D、①②④ |
铜粉放入稀硫酸溶液中,加热后无明显现象发生.当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出.该盐是( )
| A、Fe2(SO4)3 |
| B、Na2CO3 |
| C、KNO3 |
| D、FeSO4 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,则x+y=46 |
| B、1 mol氯气参加氧化还原反应,一定得到NA 或2NA个电子 |
| C、1升0.1 mol?L-1 NaBr溶液中,HBr和Br-总和为0.1NA个 |
| D、12.5 mL 16 mol?L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
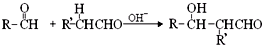 (-R、-R′表示氢原子或烃基)
(-R、-R′表示氢原子或烃基)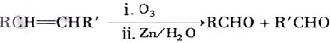
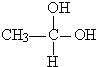 →CH3-CHO+H2O
→CH3-CHO+H2O