题目内容
3.关于维生素C的说法中不正确的是( )| A. | 易溶于水,水溶液显酸性 | B. | 受热易被氧化 | ||
| C. | 在水溶液中容易被还原 | D. | 新鲜的水果和蔬菜中含有维生素C |
分析 维生素C含有碳碳双键、醚键、羟基等官能团,含醛基的官能团能发生银镜反应,据此解题.
解答 解:A、维生素C显酸性,属于水溶性维生素,故A正确;
B、维生素C中含碳碳双键和-OH,均有还原性,故受热易氧化,故B正确;
C、维生素C中含碳碳双键和-OH,易被氧化,故C错误;
D、维生素C大量存在于新鲜水果和蔬菜中,故D正确.
故选C.
点评 本题考查有机物的结构与性质,注意习题中的信息分析物质的性质,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目
13.实验室制备1,2-二溴乙烷的反应原理如下:①CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2,②CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:①乙醇在浓硫酸的存在下在l40℃脱水生成乙醚(CH3CH2OCH2CH3);②浓硫酸将乙醇脱水碳化.
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
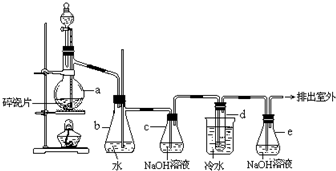
有关数据列表如下:
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置d,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
可能存在的主要副反应有:①乙醇在浓硫酸的存在下在l40℃脱水生成乙醚(CH3CH2OCH2CH3);②浓硫酸将乙醇脱水碳化.
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置d,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
14.在有机合成中,常会将官能团消除或增加,下列相关过程中反应类型及相关产物不合理的是( )
| A. | 乙烯→乙二醇:CH2═CH2$\stackrel{加成}{→}$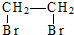 $\stackrel{取代}{→}$ $\stackrel{取代}{→}$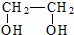 | |
| B. | 溴乙烷→乙醇:CH3CH2Br$\stackrel{消去}{→}$CH2═CH2$\stackrel{加成}{→}$CH3CH2OH | |
| C. | 1-溴丁烷→1,3-丁二烯:CH3CH2CH2CH2Br$\stackrel{消去}{→}$CH3CH2CH=CH2$\stackrel{加成}{→}$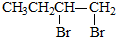 $\stackrel{消去}{→}$CH2═CH-CH═CH2 $\stackrel{消去}{→}$CH2═CH-CH═CH2 | |
| D. | 乙烯→乙炔:CH2═CH2$\stackrel{加成}{→}$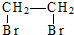 $\stackrel{消去}{→}$CH≡CH $\stackrel{消去}{→}$CH≡CH |
11.某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)?3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%.在此平衡体系中加入1molZ(g),恒定温度条件下,在平衡后X、Y、Z的体积分数不变.下列叙述正确的是( )
| A. | 第二次平衡时,Z的浓度为0.2 mol•L-1 | |
| B. | m=3 | |
| C. | X与Y的平衡转化率之比为1:2 | |
| D. | 加入Z后平衡没移动 |
18.下列物质中,含有氧分子的是( )
| A. | MnO2 | B. | CO2 | C. | H2O2 | D. | 空气 |
8.下列离子方程式正确的是( )
| A. | 工业上用石灰乳制备漂白粉:Ca(OH)2+Cl2=Ca2++ClO-+Cl-+H2O | |
| B. | 向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3•H2O+2H2O | |
| C. | 制备Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
12.NaOH溶液导电的原因是含有( )
| A. | 自由移动的分子 | B. | 自由移动的离子 | C. | 自由移动的电子 | D. | 自由移动的原子 |
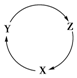 下列各组物质中,满足如图物质一步转化关系的选项是( )
下列各组物质中,满足如图物质一步转化关系的选项是( )