题目内容
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因是( )
| A、生成一种强酸弱碱盐 |
| B、弱酸溶液和强碱溶液 |
| C、弱酸与弱碱溶液反应 |
| D、一元强酸溶液与一元强碱溶液反应 |
考点:酸碱混合时的定性判断及有关ph的计算,盐类水解的应用
专题:电离平衡与溶液的pH专题
分析:若pH=3的酸溶液和pH=11的碱溶液中,c(H+)=c(OH-)=10-3mol/L,等体积混合后溶液呈酸性,说明应后酸过量,应为弱酸和强碱的反应,本题可通过讨论进行分析.
解答:
解:pH=3的酸溶液和pH=11的碱溶液中,c(H+)=c(OH-)=10-3mol/L,
①若为强酸、强碱溶液,在溶液中完全电离,则反应后溶液呈中性;
②若为弱酸、强碱溶液,弱酸在溶液中部分电离,混合后酸过量,溶液呈酸性;
③若为强酸、弱碱溶液,弱碱在溶液中部分电离出氢氧根离子,碱过量,反应后溶液呈碱性,
根据分析可知,只有B符合,
故选B.
①若为强酸、强碱溶液,在溶液中完全电离,则反应后溶液呈中性;
②若为弱酸、强碱溶液,弱酸在溶液中部分电离,混合后酸过量,溶液呈酸性;
③若为强酸、弱碱溶液,弱碱在溶液中部分电离出氢氧根离子,碱过量,反应后溶液呈碱性,
根据分析可知,只有B符合,
故选B.
点评:本题考查酸碱混合的定性判断,侧重考查弱电解质的电离和盐类的水解知识,题目难度中等,注意当c(H+)=c(OH-)时,弱电解质的浓度大于强电解质溶液的浓度,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19世纪-20世纪,德国培养和出现了很多的化学家和物理学家,如魏勒、凯库勒、拜尔、霍夫曼、李比希、爱因斯坦、普朗克、赫兹、伦琴、海森堡等.其主要原因是( )
| A、德国从小学到高中很重视学生创新能力和实验能力的培养,在大学重视理工科的教学和研究,当时柏林大学教授的工资是第一线工人工资的50倍以上 |
| B、德国从小学到高中很重视学生解题能力的培养,每天都有大量的做不完的作业,所以,在以后的工作和科研中,遇到难题均能冥思苦想,得出正确的答案 |
| C、德国从小学到高中很重视学生数学能力的培养,为学生的发展打下了扎实的数学功底,使任何问题均能用数学方法解答出来 |
| D、德国从小学到高中很重视学生英语教学,为学生的国际交流打下了扎实的语言基础 |
没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
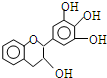

| A、分子中所有的碳原子共面 |
| B、1mol EGC与4molNaOH恰好完全反应 |
| C、易发生加成反应,难发生氧化反应和取代反应 |
| D、遇FeCl3溶液发生显色反应 |
下列溶液中的离子因发生氧化-还原反应而不能大量共存的是( )
| A、Na+、Al3+、SO42-、HCO3- |
| B、K+、Fe3+、Cl-、SCN- |
| C、Ca2+、Na+、ClO-、S2- |
| D、Ca2+、Ba2+、F-、Br- |
已知0.1mol?L-1的NaHCO3溶液的pH=8,同浓度的NaAlO2溶液的pH=11,将两种溶液等体积混合,并且发生了反应,可能较大量生成的物质是( )
| A、CO2 |
| B、Al(OH)3 |
| C、H2CO3 |
| D、Al3+ |
在相同温度和相同浓度下的各种稀溶液中,下列各项排列可能不正确的是( )
| A、溶液的酸性:H2SO4>Al2(SO4)3>NH4NO3 |
| B、溶液的pH:Na2CO3>NaHCO3>CH3COONa |
| C、由水电离出的c(OH-):NaCl>HCl>NaOH |
| D、带电微粒数:Na2S>H2SO4>Mg(OH)2 |