题目内容
下列溶液中的离子因发生氧化-还原反应而不能大量共存的是( )
| A、Na+、Al3+、SO42-、HCO3- |
| B、K+、Fe3+、Cl-、SCN- |
| C、Ca2+、Na+、ClO-、S2- |
| D、Ca2+、Ba2+、F-、Br- |
考点:离子共存问题
专题:离子反应专题
分析:A.铝离子与碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,但不属于氧化还原反应;
B.铁离子与硫氰根离子反应生成络合物硫氰化铁,不属于氧化还原反应;
C.次氯酸根离子具有强氧化性,能够氧化硫离子,钙离子与硫离子反应生成氯化钙沉淀;
D.Ca2+、Ba2+、F-、Br-离子之间不满足离子反应发生条件.
B.铁离子与硫氰根离子反应生成络合物硫氰化铁,不属于氧化还原反应;
C.次氯酸根离子具有强氧化性,能够氧化硫离子,钙离子与硫离子反应生成氯化钙沉淀;
D.Ca2+、Ba2+、F-、Br-离子之间不满足离子反应发生条件.
解答:
解:A.Al3+、HCO3-之间发生双水解反应,在溶液中不能大量共存,但该反应不是氧化还原反应,故A错误;
B.Fe3+、SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,但该反应不属于氧化还原反应,故B错误;
C.Ca2+、S2-之间发生反应生成硫化钙沉淀,ClO-能够氧化S2-,在溶液中不能大量共存,存在氧化还原反应,故C正确;
D.Ca2+、Ba2+、F-、Br-离子之间不发生反应,在溶液中能够大量共存,故D错误;
故选C.
B.Fe3+、SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,但该反应不属于氧化还原反应,故B错误;
C.Ca2+、S2-之间发生反应生成硫化钙沉淀,ClO-能够氧化S2-,在溶液中不能大量共存,存在氧化还原反应,故C正确;
D.Ca2+、Ba2+、F-、Br-离子之间不发生反应,在溶液中能够大量共存,故D错误;
故选C.
点评:本题考查离子共存的正误判断,为高考中的高频题,题目难度中等,注意掌握离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
 2008年夏季奥运会即将在我国举行,我国支持“绿色奥运、科技奥运、人文奥运”,人文奥运的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图,有关该物质的说法正确的是( )
2008年夏季奥运会即将在我国举行,我国支持“绿色奥运、科技奥运、人文奥运”,人文奥运的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图,有关该物质的说法正确的是( )| A、属于芳香烃 |
| B、属于高分子化合物 |
| C、属于苯酚的同系物 |
| D、与溴水可发生加成反应和取代反应 |
下列物质与常用危险化学品的类别不对应的是( )
| A、H2SO4、NaOH--腐蚀品 |
| B、CH4、H2--易燃液体 |
| C、白磷--易燃固体 |
| D、KMnO4、H2O2--氧化剂 |
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因是( )
| A、生成一种强酸弱碱盐 |
| B、弱酸溶液和强碱溶液 |
| C、弱酸与弱碱溶液反应 |
| D、一元强酸溶液与一元强碱溶液反应 |
某二元酸H2A在水中发生电离:H2A=H++HA-(完全电离),HA-?H++A2-.下列叙述中一定不正确的是( )
| A、在NaHA溶液中:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B、在Na2A溶液中:c(Na+)>c(A2-)>c(OH-)>c(H+) |
| C、在NaHA溶液中:c(H+)=c(A2-)+c(OH-) |
| D、在H2A溶液中:c(H+)=c(HA-)+c(OH-)+2c(A2-) |
下列能用或图装置制取气体并能“随开随用、随关随停”的是( )
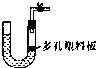

| A、锌粒和稀硫酸制取氧气 |
| B、电石和水制取乙炔 |
| C、浓盐酸和二氧化锰制取氯气 |
| D、大理石和稀硫酸制取二氧化碳 |
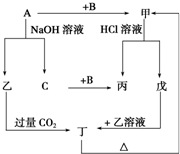 由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料.请回答:
由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料.请回答: