题目内容
8.A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示.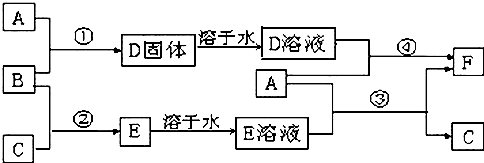
请回答:
(1)写出A与B反应的化学方程式:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3
(2)写出第④步反应的离子方程式为Fe+2Fe3+═3Fe2+.
(3)写出向F溶液中通入B时发生反应的离子方程式Cl2+2Fe2+═2Fe3++2Cl-.
(4)写出Cu与D溶液反应的离子方程式2Fe3++Cu═2Fe2++Cu2+.
(5)用离子方程式表示D溶液中滴加KSCN溶液显红色的原因Fe3++3SCN-=Fe(SCN)3.
(6)向F溶液中滴入NaOH溶液过程中发生的氧化还原反应化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3.
分析 A是用途最广的金属,则A是Fe,D溶液中滴加KSCN溶液显血红色,说明D中含有铁离子,B、C是两种常见气体单质,则B应该具有强氧化性,BC反应生成E,E溶液为常见强酸,则B是Cl2、C是H2、E是HCl、D为FeCl3,E溶液是盐酸、D溶液是氯化铁溶液,A和氯化铁溶液反应生成FeCl2,所以F是FeCl2,Fe和稀盐酸反应生成H2,据此分析解答.
解答 解:A是用途最广的金属,则A是Fe,D溶液中滴加KSCN溶液显血红色,说明D中含有铁离子,B、C是两种常见气体单质,则B应该具有强氧化性,BC反应生成E,E溶液为常见强酸,则B是Cl2、C是H2、E是HCl、D为FeCl3,E溶液是盐酸、D溶液是氯化铁溶液,A和氯化铁溶液反应生成FeCl2,所以F是FeCl2,Fe和稀盐酸反应生成H2,
(1)Fe在氯气中燃烧生成氯化铁,反应方程式为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,
故答案为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(2)Fe和氯化铁反应生成可溶性的氯化亚铁,离子方程式为Fe+2 Fe3+═3 Fe2+,
故答案为:Fe+2 Fe3+═3 Fe2+;
(3)氯气具有强氧化性,亚铁离子具有还原性,二者反应生成氯化铁,离子方程式为Cl2+2Fe2+═2Fe3++2Cl-,
故答案为:Cl2+2Fe2+═2Fe3++2Cl-;
(4)铜和氯化铁发生氧化还原反应生成氯化亚铁和氯化铜,离子方程式为2Fe3++Cu═2Fe2++Cu2+,
故答案为:2Fe3++Cu═2Fe2++Cu2+;
(5)D为氯化铁,铁离子用KSCN溶液检验,能和KSCN溶液混合生成络合物而使溶液呈血红色,离子方程式为Fe3++3SCN-=Fe(SCN)3,
故答案为:Fe3++3SCN-=Fe(SCN)3;
(6)F是氯化亚铁,氯化亚铁和NaOH反应生成白色沉淀氢氧化亚铁,氢氧化亚铁不稳定,易被空气氧化生成红褐色氢氧化铁沉淀,反应方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
点评 本题考查无机物推断,为高频考点,涉及Fe及其化合物之间的转化,知道铁离子及亚铁离子的检验方法及现象,知道氯化亚铁和氢氧化钠反应现象及氢氧化亚铁的制备方法,题目难度不大.

| A. | 14C可用于测定一些文物的年代,该过程是化学变化 | |
| B. | 烧结粘土制陶瓷是物理变化 | |
| C. | 服用阿司匹林出现水杨酸反应时,用碳酸氢钠溶液解毒是复分解反应 | |
| D. | 从海水中提取镁的过程中,发生的是非氧化还原反应 |
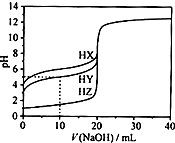 25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )| A. | 在相同温度下,同浓度的三种酸溶液的酸性强弱顺序:HZ<HY<HX | |
| B. | HZ、HY、HX均为弱酸 | |
| C. | 向HY溶液中加入10.00mLNaOH溶液,一定有c(Y-)+c(OH-)═c(H+)+c(Na+) | |
| D. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) |
| 元素 | 相关信息 |
| X | X的基态原子核外只有三个能级,且各能级电子相等 |
| Y | Y的基态原子最外层电子数是其内层电子总数的三倍 |
| Z | Z的基态原子价电子排布为nsn-1 |
| W | W的单质是一种常见的红色金属,在潮湿的空气中易生成绿色的锈斑 |
(2)与Z同周期且依次相邻的两种元素的原子与Z比较,三者第一电离能的大小顺序为I1(Mg)>I1(Al)>I1(Na)[用I1(元素符号)表示];Y的氢化物在同族的氢化物中沸点反常,其原因是水分子间存在氢键.
(3)写出W的单质在潮湿的空气中生成绿色锈斑的化学方程式,并标出电子转移的方向和数目:
 .
.(4)在X、Y与氢三种元素组成的多种分子中,有些分子的核磁共振氢谱显示有三种氢,且数目比为1:2:3,写出其中一种分子的名称:乙醇.X、Y可以形成多种弱酸根离子,写出其中一种离子水解的离子方程式:CO32-+H2O??HCO3-+OH-.
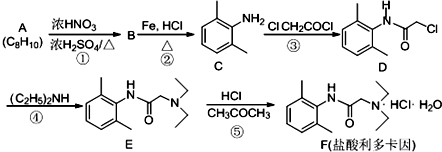
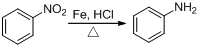
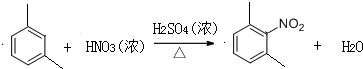 ,反应类型为取代反应,上述流程中,反应类型与①相同的还有③④(填反应序号).
,反应类型为取代反应,上述流程中,反应类型与①相同的还有③④(填反应序号). (R为烃基)
(R为烃基)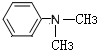 (写结构简式).
(写结构简式).
 .
. .
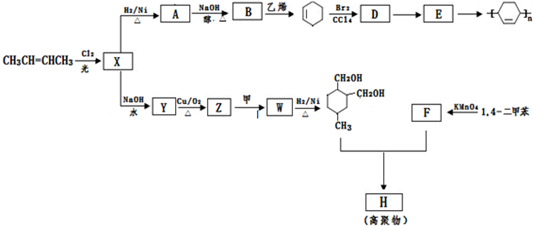
.
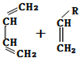 →
→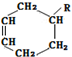 (或写成
(或写成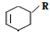 R代表取代基或氢)
R代表取代基或氢)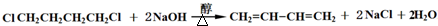 ;
;
 ;
; .
. .
.