题目内容
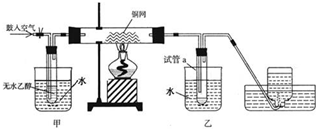
侯氏制碱法是连续循环生产的过程,主要流程见图,有关该流程的叙述中正确的是( )


A、母液中含有大量的Na+、NH
| ||||
B、通入NH3只是为了增加NH
| ||||
| C、加入的Y物质为CO2 | ||||
| D、生产过程中还需要补充水 |
考点:纯碱工业(侯氏制碱法)
专题:
分析:A、降温池中通入过量的氨气,所以母液中含有大量的氯化铵和碳酸钠,可能含有过量的氯化钠;
B、氨水溶液呈碱性,增强二氧化碳的溶解度;
C、加入的X物质为CO2,Y物质为氯化钠;
D、反应NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl中要消耗水.
B、氨水溶液呈碱性,增强二氧化碳的溶解度;
C、加入的X物质为CO2,Y物质为氯化钠;
D、反应NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl中要消耗水.
解答:
解:A、降温池中通入过量的氨气,所以母液中含有大量的氯化铵和碳酸钠,可能含有过量的氯化钠,所以母液中含有大量的Na+、NH4+、Cl-、CO32-,故A正确;
B、氨水溶液呈碱性,增强二氧化碳的溶解度,故B错误;
C、加入的X物质为CO2,Y物质为氯化钠,故C错误;
D、反应NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl中消耗水,所以生产过程中还需要补充水,故D正确;
故选AD.
B、氨水溶液呈碱性,增强二氧化碳的溶解度,故B错误;
C、加入的X物质为CO2,Y物质为氯化钠,故C错误;
D、反应NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl中消耗水,所以生产过程中还需要补充水,故D正确;
故选AD.
点评:本题考查了侯氏制碱法的原理、流程及工艺特点,题目难度不大,准确把握整个工艺流程是解题的关键.

练习册系列答案
相关题目
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y.下列说法正确的是( )
| A、还原性:X的氢化物>Y的氢化物>Z的氢化物 |
| B、简单离子的半径:M的离子>Z的离子>Y的离子>X的离子 |
| C、YX2、M2Y都是含有极性键的共价化合物 |
| D、Z元素的最高价氧化物的水化物的化学式为HZO4 |
间甲乙苯苯环上一个H原子被-C3H6Cl取代,形成的同分异构体有(不考虑立体异构)( )
| A、9种 | B、12种 |
| C、15种 | D、20种 |
NaCl是从海水中提取出来的一种重要物质,除了作调味品以外,它还是一种重要的化工原料.下列产品或物质以NaCl为主要原料制取的是( )
①金属钠; ②氯气; ③烧碱; ④盐酸; ⑤纯碱.
①金属钠; ②氯气; ③烧碱; ④盐酸; ⑤纯碱.
| A、只有①② | B、只有①②③ |
| C、只有①②③④ | D、全部 |
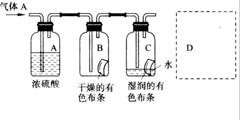 某学生用如图所示的方法研究物质的性质,其中气体A的主要成分,杂质是空气和水蒸气,回答下列问题:
某学生用如图所示的方法研究物质的性质,其中气体A的主要成分,杂质是空气和水蒸气,回答下列问题: