题目内容
CO2和CO与我们的社会生活联系非常密切,某化学课题组对此进行了探究.
(1)CO2可用NaOH溶液吸收得到碳酸盐.
①已知25℃时,C
解反应的平衡常数(即水解常数),Kb=
=2×10-4mol?L-1,当溶液中c(HC
):c(C
)=2:1时溶液的pH=
②若将0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合,则混合后的溶液中c(C
) c(HC
)(填“大于”“小于”或“等于”) 0.1mol?L-1Na2CO3溶液 中c(OH-)-c(H+)= [用c(HC
)、c(H2CO3)的关系式表示].
(2)常温常压下,饱和CO2水溶液的PH=5.6,c(H3CO3)=1.5×10-3mol?L-1,若忽略水的电离及H2CO3的第二级电离,则H2CO3?HC
+H+的平衡常数K= .(已知:10-5.6=2.5×10-6)
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(C
)(填“>”“=”“<”)原因是 (用离子方程式和必要的文字说明).
(4)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9),小李应该选用的试剂是
(5)一定条件下,将2molH2O(g)和2molCO充入容积固定的1L的密闭容器中,加热至高温,发生下列可逆反应:2H2O?2H2+O2…①2CO+O2?2CO2…②请回答下列问题:
①当容器内的压强不在发生改变时,测知下列提供的各项物理量即可求出该条件下求得该条件下混合气体平衡组成的是 (填序号,K1指①反应的平衡常数,K2指的是②反应的平衡常数)
A.K1、K2 B.K1、c(CO2) C.K2、c(CO2) D.c(CO2)、c(CO
②请在如图中,画出反应过程中的c(O2)变化曲线.

(1)CO2可用NaOH溶液吸收得到碳酸盐.
①已知25℃时,C
| O | - 3 |
c(H
| ||
c(
|
| O | - 3 |
| O | 2- 3 |
②若将0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合,则混合后的溶液中c(C
| O | 2- 3 |
| O | - 3 |
| O | - 3 |
(2)常温常压下,饱和CO2水溶液的PH=5.6,c(H3CO3)=1.5×10-3mol?L-1,若忽略水的电离及H2CO3的第二级电离,则H2CO3?HC
| O | - 3 |
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)
| O | 2- 3 |
(4)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9),小李应该选用的试剂是
(5)一定条件下,将2molH2O(g)和2molCO充入容积固定的1L的密闭容器中,加热至高温,发生下列可逆反应:2H2O?2H2+O2…①2CO+O2?2CO2…②请回答下列问题:
①当容器内的压强不在发生改变时,测知下列提供的各项物理量即可求出该条件下求得该条件下混合气体平衡组成的是
A.K1、K2 B.K1、c(CO2) C.K2、c(CO2) D.c(CO2)、c(CO
②请在如图中,画出反应过程中的c(O2)变化曲线.

考点:离子浓度大小的比较,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)①常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,先反应生成碳酸氢钠,再与盐酸反应生成二氧化碳、水,以此分析解答;
②若将0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合,碳酸根离子水解程度大于碳酸氢根离子,离子浓度碳酸氢根离子浓度大于碳酸根离子浓度;根据原子守恒和电荷守恒计算c(OH-)-c(H+)的值;
(2)电离平衡常数指弱电解质在一定条件下电离达到平衡时,溶液中电离所生成的各种离子浓度系数次幂的乘积,跟溶液中未电离分子的浓度系数次幂的乘积的比值,则H2CO3?HCO3-+H+的平衡常数K=
;
(3)依据溶液呈碱性,判断碳酸氢根离子水解程度大于电离程度分析判断离子浓度大小;
(4)根据CaCO3、BaCO3的溶度积大小可知BaCO3更难溶,因此令CO2生成BaCO3反应更完全;
(5)①两个反应靠O2联系起来,只要知道O2和另外任意一种气体的平衡浓度,均可求出混合气体的平衡组成;
②依据化学平衡计算平衡后得到氧气物质的量,结合反应过程画出变化曲线.
②若将0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合,碳酸根离子水解程度大于碳酸氢根离子,离子浓度碳酸氢根离子浓度大于碳酸根离子浓度;根据原子守恒和电荷守恒计算c(OH-)-c(H+)的值;
(2)电离平衡常数指弱电解质在一定条件下电离达到平衡时,溶液中电离所生成的各种离子浓度系数次幂的乘积,跟溶液中未电离分子的浓度系数次幂的乘积的比值,则H2CO3?HCO3-+H+的平衡常数K=
| c(H+)c(HCO3-) |
| c(H2CO3) |
(3)依据溶液呈碱性,判断碳酸氢根离子水解程度大于电离程度分析判断离子浓度大小;
(4)根据CaCO3、BaCO3的溶度积大小可知BaCO3更难溶,因此令CO2生成BaCO3反应更完全;
(5)①两个反应靠O2联系起来,只要知道O2和另外任意一种气体的平衡浓度,均可求出混合气体的平衡组成;
②依据化学平衡计算平衡后得到氧气物质的量,结合反应过程画出变化曲线.
解答:
解:(1)①水解常数Kh=
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,c(OH-)=10-4mol/L,由Kw可知,c(H+)=10-10mol/L,所以pH=10,故答案为:10;
②若将0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合,碳酸根离子水解程度大于碳酸氢根离子,离子浓度c(CO32-)<c(HCO3-),根据原子守恒和电荷守恒计算c(OH-)-c(H+)的值,根据碳原子守恒得,c(CO32-)+c(HCO3- )+c(H2CO3)=0.1mol/L,根据溶液中电荷守恒得:2×c(CO32-)+c(HCO3- )+c(OH-)=c(Na+ )+c(H+ ),c(Na+ )=0.2mol/L,所以c(OH-)-c(H+)=c(HCO3- )+2c(H2CO3),
故答案为:小于;c(HCO3- )+2c(H2CO3);
(2)饱和CO2水溶液的pH=5.6,所以c(H+)=10-5.6=2.5×10-6mol/L,c(H2CO3)=1.5×10-5 mol?L-1,
则H2CO3?HCO3-+H+的平衡常数,K=饱和CO2水溶液的pH=5.6,所以c(H+)=10-5.6=2.5×10-6mol/L,c(H2CO3)=1.5×10-5 mol?L-1,
则H2CO3?HCO3-+H+的平衡常数,K=
=
=4.2×10-7 mol?L-1,
故答案为:4.2×10-7 mol?L-1;
(3)因NaHCO3溶液显碱性,HCO3-的水解程度大于自身的电离程度,即NaHCO3溶液中既存在电离平衡为HCO3-?CO32-+H+,水解平衡为HCO3-+H2O?H2CO3+OH-,而HCO3-水解程度大于电离程度,
故答案为:>;因为NaHCO3溶液中既存在电离平衡:HCO3-?CO32-+H+,又存在水解平衡:HCO3-+H2O?H2CO3+OH-,而HCO3-水解程度大于电离程度;
(4)根据CaCO3、BaCO3的溶度积大小可知BaCO3更难溶,因此令CO2生成BaCO3反应更完全,故可选择Ba(OH)2(或NaOH溶液和BaCl2溶液)作为CO2的沉淀剂,
故答案为:Ba(OH)2(或NaOH溶液和BaCl2溶液);
(5)①由两个方程式可知,两个反应靠O2联系起来,只要知道O2和另外任意一种气体的平衡浓度,均可求出混合气体的平衡组成,当知道H2O和H2或CO和CO2的平衡浓度时,由于两个方程式无法通过O2建立反应量的关系,所以无法求其混合气体的平衡组成,选项中B符合,
故答案为:B;
②图象分析可知,水反应物质的量2mol-0.75mol=1.25mol,
2H2O=2H2 +O2
起始量(mol) 2 0 0
变化量(mol) 1.25 1.25 0.625
反应后量(mol)0.75 1.25 0.625
结合反应消耗氧气得到,
2CO+O2 ?2CO2
起始量(mol) 2 0.625 0
变化量(mol) 0.25 0.125 0.25
平衡量(mol) 1.75 0.5 0.25
最后平衡状态压强为0.5mol,图象为: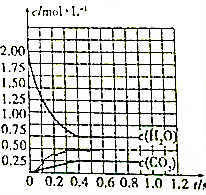 ,故答案为:
,故答案为: .
.
| c(HCO3-)c(OH-) |
| c(CO3-) |
②若将0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合,碳酸根离子水解程度大于碳酸氢根离子,离子浓度c(CO32-)<c(HCO3-),根据原子守恒和电荷守恒计算c(OH-)-c(H+)的值,根据碳原子守恒得,c(CO32-)+c(HCO3- )+c(H2CO3)=0.1mol/L,根据溶液中电荷守恒得:2×c(CO32-)+c(HCO3- )+c(OH-)=c(Na+ )+c(H+ ),c(Na+ )=0.2mol/L,所以c(OH-)-c(H+)=c(HCO3- )+2c(H2CO3),
故答案为:小于;c(HCO3- )+2c(H2CO3);
(2)饱和CO2水溶液的pH=5.6,所以c(H+)=10-5.6=2.5×10-6mol/L,c(H2CO3)=1.5×10-5 mol?L-1,
则H2CO3?HCO3-+H+的平衡常数,K=饱和CO2水溶液的pH=5.6,所以c(H+)=10-5.6=2.5×10-6mol/L,c(H2CO3)=1.5×10-5 mol?L-1,
则H2CO3?HCO3-+H+的平衡常数,K=
| c(H+)c(HCO3-) |
| c(H2CO3) |
| 2.5×10-6×2.5×10-6 |
| 1.5×10-5 |
故答案为:4.2×10-7 mol?L-1;
(3)因NaHCO3溶液显碱性,HCO3-的水解程度大于自身的电离程度,即NaHCO3溶液中既存在电离平衡为HCO3-?CO32-+H+,水解平衡为HCO3-+H2O?H2CO3+OH-,而HCO3-水解程度大于电离程度,
故答案为:>;因为NaHCO3溶液中既存在电离平衡:HCO3-?CO32-+H+,又存在水解平衡:HCO3-+H2O?H2CO3+OH-,而HCO3-水解程度大于电离程度;
(4)根据CaCO3、BaCO3的溶度积大小可知BaCO3更难溶,因此令CO2生成BaCO3反应更完全,故可选择Ba(OH)2(或NaOH溶液和BaCl2溶液)作为CO2的沉淀剂,
故答案为:Ba(OH)2(或NaOH溶液和BaCl2溶液);
(5)①由两个方程式可知,两个反应靠O2联系起来,只要知道O2和另外任意一种气体的平衡浓度,均可求出混合气体的平衡组成,当知道H2O和H2或CO和CO2的平衡浓度时,由于两个方程式无法通过O2建立反应量的关系,所以无法求其混合气体的平衡组成,选项中B符合,
故答案为:B;
②图象分析可知,水反应物质的量2mol-0.75mol=1.25mol,
2H2O=2H2 +O2
起始量(mol) 2 0 0
变化量(mol) 1.25 1.25 0.625
反应后量(mol)0.75 1.25 0.625
结合反应消耗氧气得到,
2CO+O2 ?2CO2
起始量(mol) 2 0.625 0
变化量(mol) 0.25 0.125 0.25
平衡量(mol) 1.75 0.5 0.25
最后平衡状态压强为0.5mol,图象为:
 ,故答案为:
,故答案为: .
.
点评:本题考查化学平衡的影响因素分析和计算应用,弱电解质溶液中平衡影响因素分析和PH计算,平衡常数的计算、盐类水解、图象理解应用,要能根据题目所给信息解题,善于发掘题目信息,题目难度中等.

练习册系列答案
相关题目
侯氏制碱法是连续循环生产的过程,主要流程见图,有关该流程的叙述中正确的是( )


A、母液中含有大量的Na+、NH
| ||||
B、通入NH3只是为了增加NH
| ||||
| C、加入的Y物质为CO2 | ||||
| D、生产过程中还需要补充水 |
在下列反应中,水作还原剂的是( )
| A、CaO+H2O=Ca(OH)2 |
| B、2Na+2H2O=2NaOH+H2↑ |
| C、2F2+2H2O=4HF+O2 |
| D、HCl+NaOH=NaCl+H2O |
下列物质不含有共价键的是( )
| A、Cl2 |
| B、BaCl2 |
| C、NH3 |
| D、CO2 |
X元素原子的质量数为m,核内中子数为n,则Wg X2+离子含有的电子的物质的量约为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
用铂惰性电极进行电解,下列说法正确的是( )
| A、电解饱和的食盐水,阳极产物是氢氧化钠和氯气 |
| B、电解饱和的氯化钠溶液,在阴极析出钠 |
| C、电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为2:1 |
| D、电解熔融的氯化钠,在阴极上和阳极上析出产物的物质的量之比为2:1 |

 下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①式化工生产中的一种重要固氮反应.
下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①式化工生产中的一种重要固氮反应.