��Ŀ����
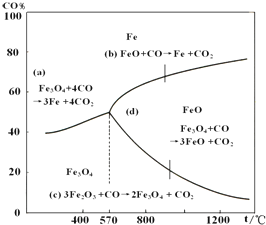 ������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯���������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ��������CO����������Ĺ�ϵ��ͼ��
������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯���������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ��������CO����������Ĺ�ϵ��ͼ����1�����¶ȵ���570��ʱ����ԭ��������ɣ����¶ȸ���570��ʱ�����η����Ļ�ԭ��Ӧ�ǣ�
��2��Ϊ���ٸ�¯����ʱ��CO��β���ŷţ������о�����ȡ����
a�������������䣬���Ӹ�¯�ĸ߶�
b�����ڻ�ԭʱ��¯��
c������ԭ���н�̿�������ı���
d�������ɵ���ˮ��ʱ�Ƴ�
��3����֪���з�Ӧ��ֵ��
��Fe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H1=-26.7kJ?mol-1
��3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g����H2=-50.8kJ?mol-1
��Fe3O4��s��+CO��g��=3FeO��s��+CO2��g����H3=-36.5kJ?mol-1
��FeO��s��+CO��g��=Fe��s��+CO2��g����H4����Ӧ�ܡ�H4=
��4��1100��ʱ����ӦFeO��s��+CO��g��?Fe��s��+CO2��g����ƽ�ⳣ��K=0.4������һ�ܱ������м���7.2g FeO��ͬʱͨ��4.48L��CO����״��������������1100�棬��ά���¶Ȳ��䣬��ƽ��ʱ��FeO��ת����Ϊ
��5�����������Ϊ21�������������Դ��Ҳ�����½�������������ԭ�������Ѳ���ʹ���ڵ�̼�ֵ������У��ü���������һ�����۵����ⷽ�����йص��Ȼ�ѧ����ʽ���£�
CH4 ��g��+0.5O2��g��?CO��g��+2H2��g����H=-36kJ?mol-1����a��
CH4 ��g��+H2O��g��?CO��g��+3H2��g����H=+216kJ?mol-1����b��
��Ϊ�ζ��÷�Ӧ��b��������
�ڹ�ҵ�Ͻ������ˮ������Ӧ��Ļ������������·�ӦCO��g��+H2O��g��?H2��g��+CO2��g��������1000���£��ù���ѹˮ����ϴ�ӻ�����壬�پ���������ֱ����Ϊ�ϳɰ���ԭ���������¸�ѹ������������
���㣺�ø�˹���ɽ����йط�Ӧ�ȵļ���,��ѧƽ��ĵ�������
ר�⣺��ѧ��Ӧ�е������仯,��ѧƽ��ר��
��������1����ͼ��֪���¶ȵ���570��ʱ��������ӦΪ3Fe2O3+CO=2Fe3O4+CO2��Fe3O4+4CO=3Fe+4CO2�����¶ȸ���570��ʱ�������Ļ�ԭ��Ӧ��3Fe2O3+CO=2Fe3O4+CO2��Fe3O4+CO=3FeO+CO2��FeO+CO=Fe+CO2��������Ԫ�صĻ��ϼ��жϷ�����Ӧ��˳��
��2��Ϊ���ٸ�¯ұ��ʱ����CO��β���ŷţ�Ӧ��ƽ��������Ӧ�ƶ�������ƽ���ƶ�������
��3�����ݸ�˹���ɹ���Ŀ���Ȼ�ѧ����ʽ��
��4����ת���ʵ�CO�����ʵ���Ϊxmol����������ʽ��x��ʾ��ƽ��ʱһ����̼�������̼��Ũ�ȣ�����ƽ�ⳣ������xֵ�����ݷ���ʽ��֪ת����FeO�����ʵ���n��FeO��=n��CO��������ת����FeO�������������ת���ʶ�����㣻
��5����a���ÿ��������������ײ���������̼�����ʣ�
�����ݻ�ѧ��Ӧ���ʺͷ�Ӧ���ת���ʣ���������ܽ��Է����ж�������ѡ��
��2��Ϊ���ٸ�¯ұ��ʱ����CO��β���ŷţ�Ӧ��ƽ��������Ӧ�ƶ�������ƽ���ƶ�������
��3�����ݸ�˹���ɹ���Ŀ���Ȼ�ѧ����ʽ��
��4����ת���ʵ�CO�����ʵ���Ϊxmol����������ʽ��x��ʾ��ƽ��ʱһ����̼�������̼��Ũ�ȣ�����ƽ�ⳣ������xֵ�����ݷ���ʽ��֪ת����FeO�����ʵ���n��FeO��=n��CO��������ת����FeO�������������ת���ʶ�����㣻
��5����a���ÿ��������������ײ���������̼�����ʣ�
�����ݻ�ѧ��Ӧ���ʺͷ�Ӧ���ת���ʣ���������ܽ��Է����ж�������ѡ��
���
�⣺��1����ͼ��֪���¶ȵ���570��ʱ��������Ӧbcd������Ԫ�صĻ��ϼ۽��Ϳ�֪�����η����Ļ�ԭ��Ӧ��
3Fe2O3+CO=2Fe3O4+CO2��Fe3O4+CO=3FeO+CO2��FeO+CO=Fe+CO2���ʷ�Ӧ˳��Ϊcdb��
�ʴ�Ϊ��cdb��
��2����a�������������䣬���Ӹ�¯�ĸ߶ȣ���Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���a����
��b����ӦΪ���ȷ�Ӧ�����ڻ�ԭʱ��¯�£�������ƽ��������Ӧ���У�����һ����̼�ĺ�������b��ȷ��
��c����̿��������ǹ��壬����ԭ���н�̿�������ı�������Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���c����
��d�����ɵ���ˮΪҺ̬�������ɵ���ˮ��ʱ�Ƴ�����Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���d����
��ѡ��acd��
��3����֪����Fe2O3��s��+3CO��g��=2Fe��s��+3CO 2��g����H1=-26.7kJ?mol-1��
��3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g����H2=-50.8kJ?mol-1��
��Fe3O4��s��+CO��g��=3FeO��s��+CO2 ��g����H3=-36.5kJ?mol-1��
�ɸ�˹���ɿ�֪���١�3-��-�ۡ�2��6FeO��s��+6CO��g��=6Fe��s��+6CO2��g����H=3��H1-��H2-2��H1��
���ԡ�H4=
��H=
��3��H1-��H2-2��H1��=
��[3����-26.7kJ?mol-1��-��-50.8kJ?mol-1��-2����-36.5kJ?mol-1��]=7.3kJ?mol-1��
�ʴ�Ϊ��7.3��
��4��4.48LCO�����ۺ�Ϊ��״�������ʵ���Ϊ
=0.2mol����ת���ʵ�CO�����ʵ���Ϊxmol����
FeO��s��+CO��g��?Fe��s��+CO2��g����
��ʼ��mol����0.2 0
�仯��mol����x x
ƽ�⣨mol����0.2-x x
һ����̼��ϵ�����ڶ�����̼��ϵ�����ʿ��������ʵ�������Ũ�ȼ���ƽ�ⳣ����
����
=0.4�����x=
mol
�ɷ���ʽ��֪��ת����FeO�����ʵ���n��FeO��=n��CO��=
mol��
����FeO��ת����Ϊ
��100%=57.1%���ʴ�Ϊ��57.1%��
��5���ٷ�Ӧa�У������������ÿ��ƣ������ɶ�����̼�����ʣ��ʴ�Ϊ��a���ÿ��������������ײ���������̼�����ʣ�
��CO��g��+H2O��g��?H2 ��g��+CO2��g����H��0������1000���£��ù���ѹˮ����ϴ�ӻ�����壬�پ���������ֱ����Ϊ�ϳɰ���ԭ��������ѹ���´����������Ǹ�����������߷�Ӧ���ʣ�����ѹˮ����������ƽ��������У����һ����̼ת���ʣ����ɵĶ�����̼�е��ܽ��ԣ�
�ʴ�Ϊ��������������߷�Ӧ���ʣ�����ѹˮ����������COת���������Ҷ�����̼��ˮ�е��ܽ��Ҳ����
3Fe2O3+CO=2Fe3O4+CO2��Fe3O4+CO=3FeO+CO2��FeO+CO=Fe+CO2���ʷ�Ӧ˳��Ϊcdb��
�ʴ�Ϊ��cdb��
��2����a�������������䣬���Ӹ�¯�ĸ߶ȣ���Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���a����
��b����ӦΪ���ȷ�Ӧ�����ڻ�ԭʱ��¯�£�������ƽ��������Ӧ���У�����һ����̼�ĺ�������b��ȷ��
��c����̿��������ǹ��壬����ԭ���н�̿�������ı�������Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���c����
��d�����ɵ���ˮΪҺ̬�������ɵ���ˮ��ʱ�Ƴ�����Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���d����
��ѡ��acd��
��3����֪����Fe2O3��s��+3CO��g��=2Fe��s��+3CO 2��g����H1=-26.7kJ?mol-1��
��3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g����H2=-50.8kJ?mol-1��
��Fe3O4��s��+CO��g��=3FeO��s��+CO2 ��g����H3=-36.5kJ?mol-1��
�ɸ�˹���ɿ�֪���١�3-��-�ۡ�2��6FeO��s��+6CO��g��=6Fe��s��+6CO2��g����H=3��H1-��H2-2��H1��
���ԡ�H4=
| 1 |
| 6 |
| 1 |
| 6 |
| 1 |
| 6 |
�ʴ�Ϊ��7.3��
��4��4.48LCO�����ۺ�Ϊ��״�������ʵ���Ϊ
| 4.48L |
| 22.4L/mol |
FeO��s��+CO��g��?Fe��s��+CO2��g����
��ʼ��mol����0.2 0
�仯��mol����x x
ƽ�⣨mol����0.2-x x
һ����̼��ϵ�����ڶ�����̼��ϵ�����ʿ��������ʵ�������Ũ�ȼ���ƽ�ⳣ����
����
| x |
| 0.2-x |
| 2 |
| 35 |
�ɷ���ʽ��֪��ת����FeO�����ʵ���n��FeO��=n��CO��=
| 2 |
| 35 |
����FeO��ת����Ϊ
| ||
| 7.2g |
��5���ٷ�Ӧa�У������������ÿ��ƣ������ɶ�����̼�����ʣ��ʴ�Ϊ��a���ÿ��������������ײ���������̼�����ʣ�
��CO��g��+H2O��g��?H2 ��g��+CO2��g����H��0������1000���£��ù���ѹˮ����ϴ�ӻ�����壬�پ���������ֱ����Ϊ�ϳɰ���ԭ��������ѹ���´����������Ǹ�����������߷�Ӧ���ʣ�����ѹˮ����������ƽ��������У����һ����̼ת���ʣ����ɵĶ�����̼�е��ܽ��ԣ�
�ʴ�Ϊ��������������߷�Ӧ���ʣ�����ѹˮ����������COת���������Ҷ�����̼��ˮ�е��ܽ��Ҳ����
���������⿼�鷶Χ�㡢��Ŀ�Ѷȴ�ע���ͼ�����ȷ����������ʽ����ƽ������е�Ӧ�ã�

��ϰ��ϵ�д�
 Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
�����Ŀ
��֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=1.0��10-16�����й��ڲ�����֮��ת����˵���д�����ǣ�������
| A��Ksp��AgI��С��Ksp��AgCl��g��AgI����ת��ΪAgCl | ||||
| B�������������Ksp���Խ���������Խ����ת��Ϊ�����ܵ������� | ||||
| C��AgI��AgCl��������ˮ������AgCl����ת��ΪAgI | ||||
D�������£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻����
|
�������ӷ���ʽ�漰�ķ�Ӧ����������ԭ��Ӧ���ǣ�������
| A��Ba2++SO42-�TBaSO4�� |
| B��Fe+2H+�TFe2++H2�� |
| C��Al2O3+6H+�T2Al3++3H2O |
| D��HCO3-+OH-�TCO32-+H2O |
��֪25��ʱ��AgCl���ܶȻ�Ksp=1.8��10-10��������˵����ȷ���ǣ�������
| A���¶�һ��ʱ������Һ��c��Ag+����c��Cl-��=Kspʱ������ҺΪAgCl�ı�����Һ |
| B��AgNO3��Һ��NaCl��Һ��Ϻ����Һ�У�һ����c��Ag+��=c��Cl-�� |
| C����AgClˮ��Һ�м������ᣬKspֵ��� |
| D��������AgCl���뵽��Ũ��KI��Һ�У�����AgClת��ΪAgI��AgCl�ܽ��С��AgI |



 ����һ���Ĺ�ѧ���ԣ������о�����ʹ������ʧȥ��ѧ���Եķ���
����һ���Ĺ�ѧ���ԣ������о�����ʹ������ʧȥ��ѧ���Եķ���