题目内容
已知25℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是( )
| A、温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液为AgCl的饱和溶液 |
| B、AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) |
| C、向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| D、将固体AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,AgCl溶解度小于AgI |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.当溶液中c(Ag+)×c(Cl-)=Ksp时,存在溶解平衡;
B.AgNO3溶液与NaCl溶液混合硝酸银和氯化钠的物质的量不同时,混合溶液中银离子浓度和氯离子浓度不相同;
C.Ksp值只与温度有关;
D.AgCl溶解度大于AgI.
B.AgNO3溶液与NaCl溶液混合硝酸银和氯化钠的物质的量不同时,混合溶液中银离子浓度和氯离子浓度不相同;
C.Ksp值只与温度有关;
D.AgCl溶解度大于AgI.
解答:
解;A.温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,说明溶液中存在沉淀溶解平衡状态,所以此溶液为AgCl的饱和溶液,故A正确;
B.AgNO3溶液与NaCl溶液混合后的溶液中;不一定有c(Ag+)=c(Cl-),混合溶液中阴银子浓度和氯离子浓度大小,取决于硝酸银和氯化钠的相对量大小,故B错误;
C.向饱和AgCl水溶液中加入盐酸,氯离子浓度增大,沉淀溶解平衡左移形成沉淀,但温度一定.溶度积常数不变,所以Ksp值不变,故C错误;
D.将固体AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,AgCl溶解度大于AgI,沉淀向更难溶的方向进行,故D错误;
故选A.
B.AgNO3溶液与NaCl溶液混合后的溶液中;不一定有c(Ag+)=c(Cl-),混合溶液中阴银子浓度和氯离子浓度大小,取决于硝酸银和氯化钠的相对量大小,故B错误;
C.向饱和AgCl水溶液中加入盐酸,氯离子浓度增大,沉淀溶解平衡左移形成沉淀,但温度一定.溶度积常数不变,所以Ksp值不变,故C错误;
D.将固体AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,AgCl溶解度大于AgI,沉淀向更难溶的方向进行,故D错误;
故选A.
点评:本题考查了沉淀溶解平衡,为高频考点,侧重于学生的分析能力的考查,注意溶度积常数只与温度有关,沉淀可以实现沉淀转化,题目难度中等.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
实验室中利用复分解反应制取Mg(OH)2.实验数据和现象如下表所示(溶液体积均取用1mL)
关于以上实验的说法正确是( )
| 组别 | 药品1 | 药品2 | 实验现象 |
| Ⅰ | 0.1mol/LNaOH溶液 | 0.1mol/LMgCl2溶液 | 生成白色沉淀 |
| Ⅱ | 0.1mol/L氨水 | 0.1mol/LMgCl2溶液 | 无现象 |
| Ⅲ | 1mol/L氨水 | 1mol/LMgCl2溶液 | 现象Ⅲ |
| Ⅳ | 1mol/L氨水 | 0.1mol/LMgCl2溶液 | 生成白色沉淀 |
| Ⅴ | 0.1mol/L氨水 | 1mol/LMgCl2溶液 | 无现象 |
| A、实验Ⅱ、Ⅴ无现象,而Ⅳ生成白色沉淀,说明增大c(Mg2+)不能向生成沉淀的方向移动,增大氨水溶液的浓度才能向生成沉淀的方向移动 |
| B、实验Ⅲ无现象,因为氯化镁溶液和氨水浓度都增大,则导致氯化铵浓度增大,而氢氧化镁可以溶解在氯化铵溶液中 |
| C、由于氢氧化镁可以溶解在氯化铵溶液中,而氯化镁溶液和氨水反应可以生成氯化铵,所以该两种溶液混合后可能会出现先生成沉淀后溶解的现象 |
| D、实验Ⅲ的现象是生成白色沉淀,因为增大两种溶液中任意一种的浓度,都能使混合液的离子积达到氢氧化镁的Ksp |
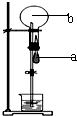 a表示胶头滴管中的液体,b表示烧瓶中的气体.不能形成喷泉实验现象的a中液体和b中气体的组合是( )
a表示胶头滴管中的液体,b表示烧瓶中的气体.不能形成喷泉实验现象的a中液体和b中气体的组合是( )| A、a-NaOH溶液、b-HCl气体 |
| B、a-NaOH溶液、b-CO2气体 |
| C、a-HCl溶液、b-NH3气体 |
| D、a-水、b-CO2气体 |
 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )| A、MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B、a点可表示MnCO3的饱和溶液,且c(Mn2+)<c(CO32-) |
| C、b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D、c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-) |
常温下,AgCl、AgBr、AgI的溶度积常数(Ksp)依次为1.8×10-10、5.0×10-13、8.3×10-17,下列有关说法错误的是( )
| A、常温下在水中溶解能力AgCl>AgBr>AgI |
| B、在AgCl饱和溶液中加入足量浓NaBr溶液有AgBr沉淀生成 |
| C、在AgBr饱和溶液中加入足量浓NaCl溶液不可能有AgCl沉淀生成 |
| D、在AgI饱和溶液中加入NaI固体有AgI沉淀析出 |
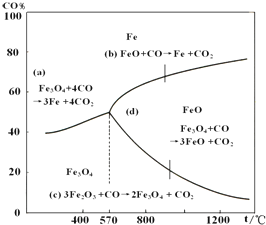 钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉炼铁,常用赤铁矿、焦炭、空气与熔剂(石灰石)作原料.已知赤铁矿被还原剂还原是逐级进行的,还原时温度及CO、CO2平衡混合气中CO的体积分数的关系如图:
钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉炼铁,常用赤铁矿、焦炭、空气与熔剂(石灰石)作原料.已知赤铁矿被还原剂还原是逐级进行的,还原时温度及CO、CO2平衡混合气中CO的体积分数的关系如图: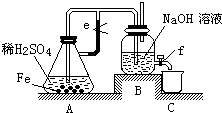
 火力发电厂释放出的大量氧化物(NOx)、SO2、CO2会对环境造成污染.对这些废气进行脱硝、脱碳和脱硫处理,可达到节能减排、废物利用等目的.
火力发电厂释放出的大量氧化物(NOx)、SO2、CO2会对环境造成污染.对这些废气进行脱硝、脱碳和脱硫处理,可达到节能减排、废物利用等目的.