题目内容
3.如图所示的下列有关实验原理或操作正确的是( )| A. |  溶解食盐 | B. | 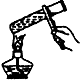 蒸发结晶 | C. |  进行定容 | D. | 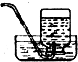 收集NO2 |
分析 A.搅拌可加速溶解;
B.液体的体积不能超过试管容积的$\frac{1}{3}$;
C.读数时,平视液面;
D.二氧化氮能与水反应.
解答 解:A.用玻璃棒搅拌可加速溶解,故A正确;
B.加热时,液体的体积不能超过试管容积的$\frac{1}{3}$,故B错误;
C.读数时,平视液面,仰视体积偏大,浓度偏小,故C错误;
D.二氧化氮能与水反应生成一氧化氮,不能用排水法收集,故D错误.
故选A.
点评 本题考查化学实验的基本操作,题目难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
13.在含有NH4Cl、AlCl3、FeCl2、FeCl3的溶液中,加入过量的NaOH溶液,微热,充分反应后再加入过量的稀盐酸,溶液中离子数目不变的是( )
| A. | NH4+ | B. | Al3+ | C. | Fe2+ | D. | Fe3+ |
14.实验中的下列操作正确的是( )
| A. | 将试剂瓶中的Na2CO3溶液倒入试管,发现取量过多,将过量的试剂倒回试剂瓶中 | |
| B. | 将含有Ba(NO3)2的废液倒入指定的容器中回收 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,立刻转移到容量瓶中 |
11.下列有关说法不正确的是( )
| A. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 | |
| B. | 金属阳离子被还原不一定得到金属单质 | |
| C. | 铝在纯氧气中能剧烈燃烧,火星四射,生成熔融的氧化铝 | |
| D. | 生铁、普通钢和不锈钢中的含碳量依次降低 |
8.将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中缓慢逐滴加入浓度为 0.1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )
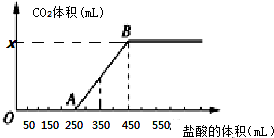

| A. | OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- | |
| B. | 当加入350 mL盐酸时,产生CO2的体积为224 mL(标准状况) | |
| C. | x点对应的数值是448 | |
| D. | 混合物中NaOH的质量为1克 |

 ,其结构和物理性质和苯相似,称为“无机苯”,该物质的二氯代物有4种.
,其结构和物理性质和苯相似,称为“无机苯”,该物质的二氯代物有4种.