题目内容
 “洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.(1)已知:
C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1 ①
2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ?mol-1 ②
C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ?mol-1 ③
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=
(2)密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g);CO的平衡转化率(a)与温度、压强的关系如图所示.
①若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为VAL,则该温度下的平衡常数K=
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA
③在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是
A 降温 B 加压 C 使用催化剂 D 将甲醇从混合体系中分离出来.
考点:用盖斯定律进行有关反应热的计算,化学平衡的影响因素,转化率随温度、压强的变化曲线
专题:化学反应中的能量变化,化学平衡专题
分析:(1)依据热化学方程式和盖斯定律来计算得到;依据n=
计算物质的量结合化学方程式的电子转移计算;
(2)①A、B点是同温度下的平衡,转化率变化,但平衡常数不变,结合化学平衡三段式列式计算A处的平衡常数,A点一氧化碳转化率为50%,B点一氧化碳转化率为70%;
②C点温度高速率达,达到平衡所需要的时间短;
③提高CO的转化率可采取的措施是改变条件促使平衡正向进行.
| V |
| V m |
(2)①A、B点是同温度下的平衡,转化率变化,但平衡常数不变,结合化学平衡三段式列式计算A处的平衡常数,A点一氧化碳转化率为50%,B点一氧化碳转化率为70%;
②C点温度高速率达,达到平衡所需要的时间短;
③提高CO的转化率可采取的措施是改变条件促使平衡正向进行.
解答:
解:(1)C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol①
C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ/mol②
由盖斯定律①-②得到CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g)△H=-524.8KJ/mol;
在标准状况下,33.6L的煤炭合成气物质的量为1.5mol,与氧气完全反应生成CO2和H2O,反应过程中2mol合成气完全反应电子转移4mol,所以1.5mol合成气反应转移电子3mol;
故答案为:-524.8; 3;
(3)CO(g)+2H2(g)?CH3OH(g),图象分析温度越高,一氧化碳转化率减小,逆向进行,正反应是放热反应;
①依据图象分析可知AB是同温度下的平衡,平衡常数随温度变化,所以平衡常数不变,A点一氧化碳转化率为50%,B点一氧化碳转化率为70%,密闭容器中充有10mol CO与20mol H2,A点平衡常数结合平衡三段式列式计算;
CO(g)+2H2 (g)?CH3OH(g)
起始量(mol) 10 20 0
变化量(mol) 5 10 5
平衡量(mol) 5 10 5
平衡常数K=
=
L2/mol2;
B点一氧化碳转化率为70%,
则 CO(g)+2H2 (g)?CH3OH(g)
起始量(mol) 10 20 0
变化量(mol) 7 14 7
平衡量(mol) 3 6 7
A、B两点时容器中,n(A)总:n(B)总=(5+10+5):(3+6+7)=20:16=5:4;
故答案为:
L2/mol2;5:4;
②达到A、C两点的平衡状态所需的时间,C点温度高反应速率快达到反应速率需要的时间短,tA>tC,故答案为:大于;
③反应是气体体积减小的放热反应,提高CO的转化率可采取的措施是降温、加压、分离出甲醇,故答案为:ABD.
C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ/mol②
由盖斯定律①-②得到CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g)△H=-524.8KJ/mol;
在标准状况下,33.6L的煤炭合成气物质的量为1.5mol,与氧气完全反应生成CO2和H2O,反应过程中2mol合成气完全反应电子转移4mol,所以1.5mol合成气反应转移电子3mol;
故答案为:-524.8; 3;
(3)CO(g)+2H2(g)?CH3OH(g),图象分析温度越高,一氧化碳转化率减小,逆向进行,正反应是放热反应;
①依据图象分析可知AB是同温度下的平衡,平衡常数随温度变化,所以平衡常数不变,A点一氧化碳转化率为50%,B点一氧化碳转化率为70%,密闭容器中充有10mol CO与20mol H2,A点平衡常数结合平衡三段式列式计算;
CO(g)+2H2 (g)?CH3OH(g)
起始量(mol) 10 20 0
变化量(mol) 5 10 5
平衡量(mol) 5 10 5
平衡常数K=
| ||||
|
| V2 |
| 100 |
B点一氧化碳转化率为70%,
则 CO(g)+2H2 (g)?CH3OH(g)
起始量(mol) 10 20 0
变化量(mol) 7 14 7
平衡量(mol) 3 6 7
A、B两点时容器中,n(A)总:n(B)总=(5+10+5):(3+6+7)=20:16=5:4;
故答案为:
| V2 |
| 100 |
②达到A、C两点的平衡状态所需的时间,C点温度高反应速率快达到反应速率需要的时间短,tA>tC,故答案为:大于;
③反应是气体体积减小的放热反应,提高CO的转化率可采取的措施是降温、加压、分离出甲醇,故答案为:ABD.
点评:本题考查了热化学方程式和盖斯定律的计算应用,化学平衡标志判断,图象分析,影响平衡的因素分析判断,化学平衡移动原理是解题关键,题目难度中等.

练习册系列答案
相关题目
已知H2(g)、CO(g)、CH3OH(l)的燃烧热△H分别是-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.下列有关叙述正确的是( )
| A、甲醇不完全燃烧生成CO和液态水的热化学方程式:CH3OH(l)+O2 (g)═CO(g)+2H2O(l)△H1=-1009.5kJ?mol-1 |
| B、已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 |
| C、2H2O(g)═2H2(g)+O2(g)△H1=+571.6 kJ?mol-1 |
| D、△H>0的化学反应在高温条件下才能自发进行 |
一定条件下,体积为10L的密闭容器中,2mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.001mol/(L?S) | ||
B、将容器体积变为20L,Z的平衡浓度变为原来的
| ||
| C、若压强增大1倍,则物质Y的转化率增大1倍 | ||
| D、若升高温度,X的浓度增大,则该反应的△H>0 |
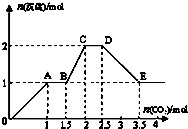 现有易溶强电解质的混合溶液10L,其中可能含有K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示:请回答下列问题:
现有易溶强电解质的混合溶液10L,其中可能含有K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示:请回答下列问题: